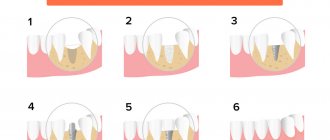
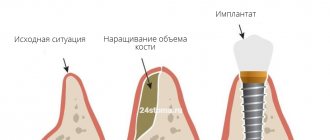
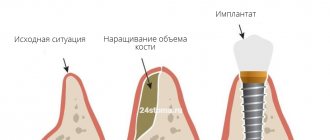
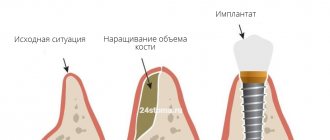
Встречающаяся в природе минеральная форма апатита кальция
| Гидроксиапатит | |
| Кристаллы гидроксиапатита на матрице | |
| Общий | |
| Категория | Фосфатный минерал группа апатита |
| Формула (повторяющаяся единица) | Ca 5 (PO 4 ) 3 (OH) |
| Классификация Струнца | 8.BN.05 |
| Кристаллическая система | Шестиугольный |
| Кристалл класс | Дипирамидальный (6 / м) Символ HM (6 / м) |
| Космическая группа | P 6 3 / м |
| Ячейка | а = 9,41 Å, с = 6,88 Å; Z = 2 |
| Идентификация | |
| Формула массы | 502,31 г / моль |
| Цвет | Бесцветный, белый, серый, желтый, желтовато-зеленый |
| Хрустальная привычка | В виде пластинчатых кристаллов и сталагмитов, конкреций, от кристаллических до массивных корок. |
| Расщепление | Плохо на {0001} и {10 1 0} |
| Перелом | Конхоидальный |
| Упорство | Хрупкий |
| Твердость по шкале Мооса | 5 |
| Блеск | Стекловидное до полусмолистого, землистого |
| Полоса | белый |
| Прозрачность | От прозрачного до полупрозрачного |
| Удельный вес | 3,14–3,21 (измерено), 3,16 (рассчитано) |
| Оптические свойства | Одноосный (-) |
| Показатель преломления | n ω = 1.651 n ε = 1.644 |
| Двулучепреломление | δ = 0,007 |
| Рекомендации | [1] [2] [3] |
Гидроксиапатит Игольчатые кристаллы гидроксиапатита на нержавеющей стали. Снимок с растрового электронного микроскопа Тартуского университета . Наноразмерное покрытие Ca-HAp, изображение, полученное с помощью сканирующего зондового микроскопа Трехмерная визуализация половины элементарной ячейки гидроксиапатита из рентгеновской кристаллографии.
Гидроксиапатит
, также называемый
гидроксилапатитом
(
HA
), представляет собой природную минеральную форму апатита кальция с формулой Ca 5 (PO 4 ) 3 (OH), но обычно ее пишут Ca 10 (PO 4 ) 6 (OH) 2 для обозначения что элементарная ячейка кристалла состоит из двух частей . [4] Гидроксиапатит является концевым гидроксильным элементом сложной группы апатита . Ион ОН — можно заменить на фторид , хлорид или карбонат , с образованием фторапатита или хлорапатита . Он кристаллизуется в гексагональной кристаллической системе . Чистый порошок гидроксиапатита белого цвета. Однако встречающиеся в природе апатиты также могут иметь коричневый, желтый или зеленый цвет, сравнимый с изменением цвета при флюорозе зубов .
До 50% по объему и 70% по массе кости человека составляют модифицированная форма гидроксиапатита, известного как костный минерал . [5] Карбонизированный гидроксиапатит с дефицитом кальция является основным минералом, из которого состоят зубная эмаль и дентин . Кристаллы гидроксиапатита также встречаются в небольших кальцификациях в шишковидной железе и других структурах, известных как корпоративные тела или «мозговой песок». [6]
Кальций-дефицитный гидроксиапатит [ править ]
Кальций-дефицитный (нестехиометрический) гидроксиапатит, Ca 10− x
(PO 4 ) 6−
x
(HPO 4 )
x
(OH) 2−
x
(где
x
находится между 0 и 1), имеет отношение Ca / P от 1,67 до 1.5. Отношение Са / Р часто используется при обсуждении фаз фосфата кальция. [9] Стехиометрический апатит Ca 10 (PO 4 ) 6 (OH) 2 имеет соотношение Ca / P 10: 6, обычно выражаемое как 1,67. Нестехиометрические фазы имеют структуру гидроксиапатита с катионными вакансиями (Ca 2+ ) и анионом (OH -) свободные места. Места, занятые исключительно фосфатными анионами в стехиометрическом гидроксиапатите, заняты фосфатными или гидрофосфатными анионами HPO 4 2- . [9] Приготовление этих фаз с дефицитом кальция может быть получено путем осаждения из смеси нитрата кальция и диаммонийфосфата с желаемым соотношением Са / Р, например, для получения образца с соотношением Са / Р 1,6: [10 ]
9,6 Ca (NO 3 ) 2 + 6 (NH 4 ) 2 HPO 4 → Ca 9,6 (PO 4 ) 5,6 (HPO 4 ) 0,4 (OH) 1,6
Спекание этих нестехиометрических фаз приводит к образованию твердой фазы, которая представляет собой однородную смесь трикальцийфосфата и гидроксиапатита, называемую двухфазным фосфатом кальция : [11]
Ca 10−
x
(PO 4 ) 6−
x
(HPO 4 )
x
(OH) 2−
x
→ (1 —
x
) Ca 10 (PO 4 ) 6 (OH) 2 + 3
x
Ca 3 (PO 4 ) 2
Развитие стоматологии на современном этапе отмечается немалыми успехами, которые связаны с внедрением в медицинскую науку и практику теоретико-экспериментальных достижений смежных наук, в том числе материаловедения.
Известно, какую важную роль играла в последние годы аутогенная костная трансплантация, однако сегодня на первое место выходят новые материалы, в частности керамические — на основе гидроксиапатита (ГАП) и трикальцийфосфата (ТКФ).
Первое сообщение о применении биоактивной керамики на основе ГАП в качестве стимулятора остеогенеза появилось в 1920 году. Исследования данных материалов активизировались в 1960-х годах.
В 1963 в работе L. Smith и соавторов был представлен анализ изучения имплантатов из различных видов керамики как заменителей кости.
Теперь эти разработки получили новый качественный виток, что позволило расширить представление о влиянии биоактивной керамики на окружающие ткани и сформировать возможные аспекты использования в медицине, в том числе в стоматологии.
Кальций-фосфатные керамики широко используются в качестве костных субстанций благодаря тому, что они имеют близкий к кости элементный состав. Среди них наиболее распространены керамики с соотношением Са и Р от 1,5 до 1,67, что соответствует элементному составу вышеуказанных ТКФ и ГАП.
Из известного арсенала керамических материалов (корундовая керамика, эмаль, кальций-фосфатные керамики и др.) в стоматологии испытываются кальций-фосфатные керамики.
Аспекты применения гидроксиапатита и трикальцийфосфата:
- Замещение дефектов зубных рядов
- Хирургическое лечение пародонтита
- Закрытие костных дефектов после цистэктомии
- Стимуляция остеогенеза при травматическом повреждении нижней челюсти
- Реконструкция атрофированного альвеолярного гребня.
В последнем случае применение имплантатов с ГАП дает существенное преимущество по сравнению с другими методами, позволяя поддерживать высоту альвеолярного гребня в течение длительного времени.
ГАП в медицине и, в том числе в стоматологии, используется в виде монолитных и пористых образцов, гранул различных размеров, в качестве покрытия на металлические имплантаты.
Доказано, что свойства гидроксиапатита зависят от условий синтеза, в первую очередь от температурного режима производства. ГАП, синтезированный при комнатной температуре, характеризуется высокими сорбционными свойствами и резорбцией.
Высокотемпературный керамический материал устойчив к факторам биологического окружения. Большое влияние на свойства керамического материала имеют различные добавки, такие как ионы различных металлов.
ТКФ керамики в чистом виде до сих пор практически используются только при экспериментальных исследованиях. Известны немногочисленные клинические разработки, где трикальцийфосфат применяется как дополнение к гидроксиапатитной керамике.
Существующие обзоры литературы освещают отдельные аспекты использования керамических материалов в стоматологии. Однако отсутствует теоретическая база, которая позволяла на основе раскрытия биологических эффектов биокерамики на кость обосновать направления клинического применения керамических материалов в стоматологии.
Цель сегодняшней статьи — рассмотреть данные по проблеме костной керамопластики и механизмов биологического взаимодействия керамических имплантатов и костной ткани.
Применение гидроксиапатита в стоматологии
Первая проблема, с которой встречается исследователь и врач, используя ГАП при научных разработках или лечении — это большое разнообразие материалов, которые объединяются под зонтичным термином «гидроксиапатит».
Методами дифрактометрии и электронной микроскопии показано, что ГАП имеет различные физико-химические характеристики фазовых состояний в зависимости от условий синтеза.
При проведении синтеза при комнатной температуре, синтетический ГАП характеризуется низкой кристалличностью. Он имеет высокие сорбционные свойства и легко всасывается в биологических средах.
Применяя такие формы ГАП, хирург имеет возможность в короткие сроки достичь заживления костных дефектов на основе стимуляции репаративного потенциала костной ткани.
При этом происходит постепенная биодеградация гидроксиапатита и замещение его новообразованной костью. Этому способствует насыщение среды кальцием и фосфором, которые высвобождаются при резорбции ГАП.
Особенно быстро идет процесс перестройки имплантата с образованием костной ткани при совместном использовании керамических материалов и биологически активных веществ.
ГАП в конденсационно-кристаллизационной форме (низкотемпературная плотная керамика) химически стабильный, практически нерастворимый в воде и обладает чрезвычайно низкой растворимость в биологических средах.
Плотность блоков такого вида ГАП керамики можно довести практически до максимального (теоретически расчитанного) значения плотности компактной керамики 3,16 г/см, что очень важно при длительных нагрузках.
Материал с такими свойствами используют для изготовления эндопротезов при замещении повреждений костей значительной длины, при зубном протезировании, достигая при этом не только восстановление формы, но и функциональной способности костного органа.
Порошкообразный ГАП, в зависимости от методики синтеза, может быть аморфным, поликристаллическим или с низкой степенью кристалличности.
Мелкодисперсный гидроксиапатит химически инертен отличается низкую растворимостью в воде, а также высокой сорбционной активностью.
Структурная организация кристаллов керамики влияет на процесс перестройки в костной ткани. В связи с этим для понимания биологической активности керамического материала необходимо знать его химический состав и кристаллическую структуру.
Рентгеноструктурный анализ демонстрирует, что большинство коммерческих препаратов гидроксиапатита не является чистыми веществами.
ГАП является структурным аналогом минерального компонента костной ткани и имеет уникальное биологическую сродство при имплантации в костную ткань. Для него характерно отсутствие соединительной ткани, обычно формирующейся вокруг инородного тела (металлического или пластикового имплантата).
Процесс остеогенеза осуществляется непосредственно на поверхности керамического материала и оценивается как остеотропное свойство биоактивного гидроксиапатита.
В литературе предоставлены тканевые, клеточные и субклеточные доказательства взаимодействия кости и гидроксиапатита. Установлено, что остеобласты в культуре ткани плотно прикрепляются к поверхности ГАП за счет образования фокальных контактов плазматической мембраны.
При этом они сохраняют биосинтетическую активность, продуцируя компоненты органического матрикса — гликозаминогликаны, коллаген, остеопонтин и другие.
Образование коллагеновых волокон наблюдается на поверхности ГАП. Их минерализация проходит за счет преципитации кристаллов ГАП, ионного обмена и за счет везикул матрикса.
По электронной микроскопии был доказан прямой контакт между кристаллами гидроксиапатита костной ткани и кристаллами ГАП имплантата.
В литературе рассматриваются два механизма образования костной ткани в условиях имплантации гидроксиапатита. Первый основан на наблюдениях, которые подтверждают, что источником регенерации является камбиальные клетки эндоста, костного мозга или другие.
В экспериментах на животных подтверждено, что костные клетки образуют компоненты межклеточного матрикса, в том числе минеральный компонент (ГАП), непосредственно из материала имплантата вследствие протекающих химических реакций.
Это обеспечивает биоактивным керамикам способность к биодеградации. Данное свойство позволяет рассматривать ГАП как «депо кальция» при ремоделирования костной ткани.
Другой, альтернативный, механизм репаративной регенерации костной ткани вокруг гидроксиапатитной керамики предполагает, что кристаллы ГАП выполняют роль «ловушки» биологически активных веществ, в частности, морфогенетического белка, значение которого в стимуляции остеогенеза научно доказано.
В основу механизма образования кости положены наблюдения авторов по кинетике формирования остеоида вокруг фрагментов дентина и гранул ГАП. Показано, что наиболее активный процесс остеогенеза наблюдался вокруг фрагментов дентина, имеющих в своем составе морфогенетический белок; несколько в меньшей степени вокруг ГАП, который, по предположению ученых, «притягивает» морфологические белки.
Описанное явление характерно как для резорбируемого гидроксиапатита, так и для форм ГАП, которые не имеют такого свойства, однако в разные сроки наблюдения.
Экспериментально доказано, что образование кости на границе ГАП происходит более интенсивно вблизи источников остеогенного роста (костный мозг и эндостальная часть кости). При их удалении интенсивность костной регенерации снижается.
Поэтому крупные костные дефекты при заполнении их гранулами керамики заживают медленнее, чем при использовании имплантата в виде резорбируемого блока ГАП или при сочетании гранул гидроксиапатита с аутотрансплантатами губчатых костей для реконструкции альвеолярного гребня нижней челюсти.
Следует отметить важность подбора величины гранул гидроксиапатита, который используется для имплантации. Так, показано, что при заполнении костных дефектов ГАП с порами размерами около 100 мкм, площадь новой костной ткани через 12 недель превышала вдвое такую же в дефектах контрольных животных.
При использовании подобного гранулята ГАП при хирургическом лечении очагов деструкции и костных дефектов в альвеолярном гребне достигается быстрое и полное заживление.
При имплантации пористых гранул гидроксиапатита наблюдается более выраженный процесс костного образования, чем при использовании компактных гранул.
При использовании гранул меньше 25 мкм наблюдается стимуляция костной резорбции за счет утилизации керамических частиц активными макрофагами. Показано, что активность макрофагов повышается при поглощении частиц латекса. При этом активизируется и резорбция кости, которая в 15 раз превышает резорбцию с участием неактивированных макрофагов.
Такое явление было продемонстрировано в культуре тканей при культивировании макрофагов и частиц металла. Механизм активации макрофагов необходимо учитывать при выборе гранулярных форм керамики для создания композитов.
В стоматологии гидроксиапатит используется не только в виде гранул, порошка и блоков плотных керамик. В медицинской практике часто возникает необходимость в применении пористых керамических имплантатов.
При соответствующей механической прочности пористая структура содержит определенное количество микропустот, создает благоприятные условия для циркуляции интерстициальной жидкости и прорастания костной ткани.
При увеличении диаметра пор прочностные характеристики керамики снижаются. Компенсация падения прочностных может быть достигнута за счет насыщения материала пластиком, который растворяется в интерстициальной жидкости.
Таким простым способом можно увеличить показатели прочности в 2-3 раза.
Имплантаты из пористой резорбируемой керамики могут служить как структурным каркасом, так и источником кальция и фосфора при замещении костной ткани.
Положительным свойством пористых керамик является то, что скорость формирования костной ткани вокруг них значительно выше, чем вблизи монолитных.
При изучении процесса остеогенеза в пористой керамике с порами различной величины было показано, что интенсивность остеогенеза максимальная при порах диаметром 90-180 мкм.
Отклонение в сторону уменьшения или увеличения величины пор приводило к резкому торможению процесса остеогенеза. Наиболее интенсивно процессы протекали в течение первого месяца, после этого они заметно снижались.
R. Bucholz и соавторы показали, что при использовании пористых кальций-фосфатних керамик имеет значение и направление расположения пор в имплантате.
Одним из перспективных направлений использования кальций-фосфатных керамик является замещение гидроксильных групп в молекуле гидроксиапатита разными ионами, придающими ГАП новые свойства.
Существуют публикации об использовании ГАП с замещением ионом F- гидроксильной группы. Применение таких форм гидроксиапатита обусловлено возможной ролью фтора в профилактике кариеса зубов.
Внедрение существующих на сегодня гидроксиапатитных керамик в стоматологии сдерживается недостаточно высокими показателями их прочности. Изучаются новые методы повышения прочности путем введения в ГАП (при замещении гидроксильной группы) ионов магния, стронция, бария, железа и хлора.
Однако вопрос перестройки костной ткани в условиях применения ГАП при замещении в его молекуле отдельных гидроксильных групп ионами металлов требует дальнейших разработок.
Несмотря на значительный процент положительных результатов в экспериментальных исследованиях и клинических испытаниях ГАП, есть и неудовлетворительные результаты.
Так, при поднадкостничном введении гидроксиапатита для реконструкции гребня альвеолярного отростка, в отдаленный период (1-3 года) отмечается резорбция и миграция имплантата, некротические изменения тканей над ним, воспаление, расхождение швов, выраженный болевой синдром.
В некоторых исследованиях имела место адгезия костной ткани и керамического остеопластического материала за счет заполнения пор костной тканью.
Применение трикальцийфосфата в стоматологии
Другой разновидностью кальций-фосфатных керамик является ТКФ.
Оптимальным составом трикальцийфосфата считается соотношение СаО и РО — 3:1. ТКФ такого состава характеризуется более высокой кинетикой рассасывания по сравнению с ГАП, который также способен резорбироваться.
Однако при оценке других соотношений (2:1 и 4:1) определено, что образцы из них слабо резорбируются. Для ТКФ характерны практически все вышеупомянутые для ГАП свойства, включая высокую биосовместимость, остеотропность, резорбция.
Дополнительное введение различных химических элементов может существенно изменить перечисленные свойства. Характеристики прочности, как и в ГАП, связаны с размером пор, или процентом пористости и в большинстве случаев недостаточны, чтобы выдерживать значительные механические нагрузки.
Считается возможным применение ТКФ для заполнения костных кист, дефектов после удаления опухолей, деструктивных полостей длинных костей и тел позвонков.
Однако до настоящего времени опубликовано только небольшое количество экспериментальных исследований. Eikenrauller и коллеги показали, что при имплантации мелкогранулярная ТКФ в дефект челюсти диаметром 4-5 мм. Уже к 4-й недели керамический материал полностью деградирует, и дефект замещается новообразованной костной тканью.
Сравнительный анализ перестройки ТКФ и аутокости показал, что место имплантации керамики в телах позвонков кролика замещается костью быстрее (6 недель) по сравнению с группой контрольных животных, у которых использовали аутокость. Через 6 недель в дефекте выявлялись лишь очаги костной и фиброзной ткани.
ТКФ может быть использован в качестве добавки к ГАП в различных соотношениях.
Бифазная керамика на основе ТКФ и ГАП
К бифазной керамике относятся остеопластические материалы, которые включают гидроксиапатит и бета-трикальцийфосфат в определенных соотношениях.
Преимуществом этой разновидности материала является сочетание свойств прочности за счет ГАП и возможность формирования депо кальция за счет биодеградации ТКФ.
В зависимости от целей и задач, производители могут разрабатывать биокерамику с заданными свойствами. В литературе имеются данные по изучению перестройки костной ткани в условиях использования макропористой бифазной кальций-фосфатной керамики — при соотношении ТКФ и ГАП 35:65.
Бюдеградация керамического материала более выражена в 1-й месяц наблюдения. С увеличением срока отмечается замедление этого процесса. При увеличении процента ТКФ в составе керамического материала скорость биодеградации увеличивается до 47% от площади имплантата. При необходимости ее можно доводить до 85%.
Наряду с процессом биодеградации происходит формирование в порах керамического материала пластинчатой костной ткани.
Бифазная керамика обладает остеогенными и остеотропными свойствами, стимулирует развитие и дифференцировку клеточной бластемы.
Сравнительные анализы перестройки бифазной керамики и аллотрансплантатов показывают, что формирование костной ткани наблюдалось в более ранние сроки в условиях имплантации керамического материала.
Выводы и рекомендации
Применение гидроксиапатита открыло новый этап в стоматологии, поскольку расширило возможности биосовместимости материала имплантата и костной ткани, способствовало разработке новых методов лечения костно-деструктивных заболеваний.
Особые свойства кальций-фосфатной керамики, в том числе сродство с костной тканью, определили их применение в качестве стимуляторов остеогенеза, источников кальция и фосфора при репаративной регенерации для замещения дефектов костей и суставов.
Важным направлением в стоматологии является разработка композитных материалов и паст на основе гидроксиапатита, которые проявляют остеоиндуктивные свойства, стимулируют репаративный процесс, ингибируют воспалительный процесс, а также способствуют более плотному удержанию имплантата за счет высоких остеоинтеграционных свойств.
Биологическая функция [ править ]
Креветка-богомол [ править ]
Дубинчатые
придатки
Odontodactylus scyllarus
(креветки павлиньих богомолов) сделаны из чрезвычайно плотной формы минерала, который имеет более высокую удельную прочность; это привело к его исследованию на предмет возможного синтеза и инженерного использования. [12] Их дактильные отростки обладают отличной ударопрочностью.из-за того, что область удара состоит в основном из кристаллического гидроксиапатита, который обладает значительной твердостью. Периодический слой под ударным слоем, состоящий из гидроксиапатита с более низким содержанием кальция и фосфора (что приводит к гораздо более низкому модулю упругости), препятствует росту трещин, заставляя новые трещины менять направление. Этот периодический слой также уменьшает энергию, передаваемую через оба слоя из-за большой разницы в модулях, даже отражая часть падающей энергии. [13]
Млекопитающее / примат / человек [ править ]
Гидроксиапатит присутствует в костях и зубах ; Кость состоит в основном из кристаллов HA, вкрапленных в коллагеновый матрикс — от 65 до 70% массы кости составляет HA. Точно так же ГК составляет от 70 до 80% массы дентина и эмали зубов. В эмали матрица для HA образована амелогенинами и эмелинами вместо коллагена. [14]
Отложения гидроксиапатита в сухожилиях вокруг суставов вызывают кальцифицирующий тендинит . [15]
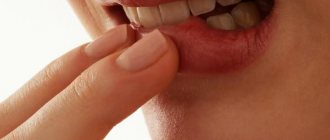
Зубные пасты без фтора для детей –
Эмаль детских зубов после их прорезывания содержит очень мало кальция, т.е. является маломинерализованной. Такая пористая эмаль очень уязвима к воздействию кариесогенных бактерий полости рта, и поэтому детские зубы особенно быстро поражаются кариесом. Зубные пасты с фтором хорошо защищают зубы от кариеса, но при необходимости выбора пасты без фтора – последняя должна обязательно содержать кальций. Лучшим соединением кальция в детских зубных пастах является нано-гидроксиапатит.
В рейтинге зубные пасты без фтора для детей, на наш взгляд, безоговорочным лидером является линейка итальянских паст PRESIDENT. Как вы увидите ниже – эти пасты обладают отличным составом и весьма приемлемой ценой. Также на наш взгляд весьма интересны пасты компании SPLAT – благодаря содержанию комплекса молочных ферментов, защищающих слизистую оболочку от стоматита и молочницы.
Зубная паста Biorepair Kids со вкусом земляники (от 0 до 6 лет) –
- производитель: Италия,
- активные вещества – 15% нано-гидроксиапатит (MicroRepair®), ионы цинка,
- абразивность – RDA 14,7,
- без фтора, лаурилсульфата и парабенов,
- туба 50 мл – от 350 до 400 рублей.
Комментарии: зубная паста Biorepair Kids содержит 15% нано-гидроксиапатит (частицы MicroRepair®, которые, как мы установили это выше – имеют размеры от 50 до 100 нанометров). По нашему мнению это лучшая детская зубная паста без фтора, предназначенная для детей от 0 до 6 лет. Кроме того, паста содержит натуральный экстракт земляники, и абсолютна безопасна при проглатывании. Ионы цинка оказывают мягкое антибактериальное действие. Высокая степень защиты от кариеса и реминерализующий эффект (который будет еще выше, если вы иногда будете комбинировать ее с фтористой зубной пастой). Внутри упаковки есть и маленький бонус – раскраска для детей.
Немного менее эффективный аналог этой зубной пасты – зубная паста KAREX Kihder (Германия), которая содержит частицы гидроксиапатита микро-размеров. Концентрация гидроксиапатита в составе этой зубной пасты – 10%, а ее противокариозная эффективность будет ниже, чем у Biorepair Kids.
Зубная паста R.O.C.S. PRO Kids «Лесные Ягоды» (от 3 до 7 лет) –
производитель – Россия,- активные вещества – гидроксиапатит, глицерофосфат кальция, хлорид магния, 10% ксилитол, экстракт жимолости,
- RDA – не указан,
- без фтора, лаурилсульфата и парабенов,
- цена за тубу 45 г – около 270 рублей.
Комментарии: неплохая зубная паста российского производителя, которая содержит микрочастицы гидроксиапатита. Кроме того производитель хитро указал, что при производстве зубной пасты использовалась 50% суспензия гидроксиапатита, но вы должны понимать, что это не имеет никакого отношения к % содержания гидроксиапатита в самой зубной пасте (кстати, производитель его не раскрывает). Также паста дополнительно содержит глицерофосфат кальция, а также хлорид магния, который ускоряет его разложение с высвобождением активных ионов кальция. Содержание ксилита безусловно также большой плюс, а экстракт жимолости окажет небольшое противовоспалительное действие.
Зубная паста SPLAT Baby «яблоко-банан» (от 0 до 3 лет) –
инструкция по применению- производитель: Россия
- содержит – гидроксиапатит, L-аргинин, комплекс молочных ферментов (лактоферрин, лактопероксидаза, лизоцим, оксидаза глюкозы), экстракт лакричника, гель Алоэ Вера,
- без фтора, лаурилсульфата и парабенов,
- цена: туба 40 мл – от 150 руб.
Комментарии: зубная паста для детей от 0 до 3 лет со вкусом яблока-банана. Содержит небольшую концентрацию гидроксиапатита, и по реминерализующему эффекту эта зубная паста будет значительно уступать первым двум. Безусловный плюс этой пасты – тут содержится комплекс молочных ферментов, который повышает местный иммунитет слизистой оболочки полости рта, что будет препятствовать развитию герпетического стоматита, а также молочницы полости рта.
Также эта паста содержит большое количество экстрактов растений и L-аргинин, которые уменьшают воспаление слизистой при прорезывании зубов. Паста полностью безопасна при случайном глотании. В комплект с пастой входит силиконовая щеточка-пальчик. В общем это весьма достойная зубная паста для детей, но по эффекту реминерализации и защиты зубов в от кариеса – она слабее первых двух. Но эта паста сильнее – в плане вопроса профилактики стоматита и грибковых инфекций полости рта у детей, а также она снижает неприятные симптомы при прорезывании зубов.
Использует [ редактировать ]
Косметика [ править ]
Гидроксиапатит добавляют в некоторые разновидности детской присыпки на основе кукурузного крахмала, такие как порошок алоэ и витамина Е от Johnson. [16] Согласно веб-сайту, минерал добавлен в качестве смягчающего средства, чтобы «помочь увлажнить и смягчить кожу». [17]
Медицинский [ править ]
Гибкий композит гидрогель-ГК, в котором соотношение минеральных и органических веществ в матрице приближается к таковому в человеческой кости.
ГК все чаще используется для изготовления материалов для костной пластики, а также для протезирования и ремонта зубов . Некоторые имплантаты, например протезы бедра , зубные имплантаты и имплантаты костной проводимости , покрыты ГК. [14] Поскольку естественная скорость растворения гидроксиапатита in vivo, около 10 мас.% В год, значительно ниже, чем скорость роста новообразованной костной ткани, при его использовании в качестве материала для замены кости, ищутся способы улучшить его степень растворимости и, таким образом, способствует лучшей биологической активности. [18]
Гидроксиапатит добавляют в специальные зубные пасты в качестве добавки для предотвращения кариеса и снижения чувствительности зубов. [19]
Дополнение [ править ]
Гидроксиапатит зарастает биоматериал
Микрокристаллический гидроксиапатит (MCHA) продается как «строящая кость» добавка с превосходной абсорбцией по сравнению с кальцием. [20]
Это добавка кальция второго поколения, полученная из бычьей кости. [20] В 1980-х годах было обнаружено, что кальциевые добавки из костной муки содержат тяжелые металлы, [20] и хотя производители заявляют, что их MCHA не содержит загрязняющих веществ, это не рекомендуется, потому что его влияние на организм не очень хорошо. -проверено. [20]
Общее использование гидроксиапатита [ править ]
В настоящее время использование гидроксиапатита или его синтетической формы, наногидроксиапатита, еще не является обычной практикой. Однако некоторые исследования показывают, что это полезно для противодействия гиперчувствительности дентина, предотвращения чувствительности после процедур отбеливания зубов и предотвращения кариеса [20] [21] [22].
Чувствительность дентина [ править ]
Нано-гидроксиапатит обладает биологически активными компонентами, которые могут ускорить процесс минерализации зубов, устраняя гиперчувствительность. Считается, что гиперчувствительность зубов регулируется жидкостью в дентинных канальцах. [20] Считается, что движение этой жидкости в результате различных стимулов возбуждает рецепторные клетки в пульпе и вызывает болевые ощущения. [20] Физические свойства наногидроксиапатита могут проникать и закрывать канальцы, останавливая циркуляцию жидкости и, следовательно, болевые ощущения от раздражителей. [21] Нано-гидроксиапатит был бы предпочтительнее, поскольку он параллелен естественному процессу реминерализации поверхности. [22]
Соагент по отбеливанию [ править ]
Средства для отбеливания зубов выделяют активные формы кислорода, которые могут разрушать эмаль. [21] Чтобы предотвратить это, в отбеливающий раствор можно добавить наногидроксиапатит, чтобы уменьшить воздействие отбеливающего агента за счет блокирования пор внутри эмали. [21] Это снижает чувствительность после отбеливания. [22]
Профилактика кариеса [ править ]
Нано-гидроксиапатит обладает реминерализующим действием на зубы и может использоваться для предотвращения повреждений от кариозных атак. [22] В случае кислотной атаки кариесогенных бактерий частицы наногидроксиапатита могут проникнуть в поры на поверхности зуба, образуя защитный слой. [21] Кроме того, наногидроксиапатит может иметь способность восстанавливать повреждения от кариозных атак, либо напрямую заменяя поврежденные поверхностные минералы, либо действуя как связывающий агент для потерянных ионов. [21]
В будущем есть возможности использования наногидроксиапатита для тканевой инженерии и восстановления. Основной и наиболее выгодной особенностью наногидроксиапатита является его биосовместимость. [23] Он химически подобен встречающемуся в природе гидроксиапатиту и может имитировать структуру и биологическую функцию структур, обнаруженных в резидентном внеклеточном матриксе. [24] Следовательно, его можно использовать в качестве основы для инженерных тканей, таких как кость и цемент. [21] Его можно использовать для восстановления расщелины губ и неба и улучшения существующих практик, таких как сохранение альвеолярной кости после удаления для лучшего размещения имплантата. [21]
Хроматография [ править ]
| В этом разделе не процитировать любые источники . Пожалуйста, помогите улучшить этот раздел , добавив цитаты из надежных источников . Материал, не полученный от источника, может быть оспорен и удален . |
Механизм хроматографии гидроксиапатита сложен и был описан как «смешанный режим». Он включает ионные взаимодействия между положительно заряженными группами на биомолекуле (часто белке) и фосфатными группами в гидроксиапатите, а также хелатирование металлов между ионами гидроксиапатита кальция и отрицательно заряженными фосфатными и / или карбоксильными группами на биомолекуле. Может быть трудно предсказать эффективность хроматографии на гидроксиапатите, основываясь на физических и химических свойствах желаемого очищаемого белка. Для элюирования обычно используется буфер с увеличивающейся концентрацией фосфата и / или нейтральной соли.
Преимущества
Филлеры с гидроксиапатитом кальция обладают многими замечательными свойствами. Среди них выделяют следующие:
- натуральность. Гомогенность и однородность препарата в сочетании с высокими профессиональными качествами врача позволяет пациенту сразу после процедуры выглядеть максимально естественно;
- ожидаемый результат. Структура геля предупреждает миграцию препарата по тканям, концентрируясь в выбранном специалистом месте;
- отсутствие отечности;
- длительный эффект. Филлер выводится из организма довольно медленно, при этом микросферы заменяются собственными, сформированными за это время тканями;
- безопасность. Препарат биосовместим с человеком, не токсичен, не вызывает аллергических реакций;
- легкая и безболезненная процедура введения;
- отсутствие реабилитационного периода;
- кожа омолаживается и оздоравливается естественным путем.
Использование в археологии [ править ]
В археологии гидроксиапатит из останков человека и животных может быть проанализирован, чтобы реконструировать древние диеты , миграции и палеоклимат. Минеральные фракции костей и зубов действуют как резервуар микроэлементов , включая углерод, кислород и стронций. Стабильный изотопный анализ гидроксиапатита человека и фауны может быть использован для определения того, была ли диета преимущественно наземной или морской (углерод, стронций); [21] географическое происхождение и миграционные привычки животного или человека (кислород, стронций) [22] и реконструировать прошлые температуры и климатические сдвиги (кислород). [23]Пост-депозиционные изменения кости могут способствовать разложению костного коллагена, белка, необходимого для анализа стабильных изотопов. [24]
Выводы
- Введение кальция гидроксиапатита в разведении в комбинации с ультразвуковым воздействием позволило стимулировать неоангиогенез, усилить синтетическую активность клеток, значительно увеличить количество волокон коллагена и эластина и ремоделировать как поверхностные, так и более глубокие слои дермы.
- Процедуры хорошо переносились, при этом высокой была степень удовлетворенности пациенток.
- Полученные результаты указывают на то, что при обработке MFU-V не нарушается, а, напротив, усиливается синтетическая активность клеток, что позволяет получить синергетический эффект при введении CaHA для улучшения подтяжки кожи.
Узнать больше об аппарате Ulthera® System можно на сайте www.pro.ulthera.ru
Дефторирование [ править ]
Гидроксиапатита является потенциальным Адсорбент для defluoridation из питьевой воды , так как она образует фторапатитовой в три этапа. Гидроксиапатит удаляет F — из воды, заменяя OH — образующий фторапатит. Однако во время процесса дефторирования гидроксиапатит растворяется и увеличивает pH и концентрацию фосфат- ионов, что делает дефторированную воду непригодной для питья. [25] Недавно была предложена технология дефторирования «гидроксиапатита с поправками на кальций» для преодоления выщелачивания фосфата из гидроксиапатита. [25] Этот метод также может повлиять на лечение флюороза путем подачи обогащенной кальцием щелочной питьевой воды на пораженные флюорозом участки.
Методы исследования
Дизайн
Рандомизированное, сравнительное клиническое исследование с обработкой разных зон разными методами (split-face) и проведением иммуногистохимического анализа.
Выборка
Девятнадцать здоровых женщин-добровольцев от 35 до 45 лет с индексом массы тела (ИМТ)
Длительность
С декабря 2015 по февраль 2022 года. Последующее наблюдение в течение 15 месяцев.
Препараты
Radiesse (Радиес) 1,5 мл, 80 шт.; препарат Radiesse 0,8 мл, 20 шт.; съемный ультразвуковой зонд/датчик DS 7 Гц — 3,0 мм, 6 шт. и DS 4 Гц – 4,5 мм, 3 шт., всего 1200 линий.
В рамках исследования было назначено пять визитов.
В 1-й и 2-й визиты (день (D)01 и месяц (M)04, соответственно) филлер (разведение физиологическим раствором 1:2) вводился подкожно в правую часть нижней трети лица, в область шеи и декольте с правой стороны и в правый нижний квадрант живота. В качестве контроля в левую часть нижней трети лица, область шеи и декольте с левой стороны вводился физиологический раствор.
В 3-й визит (М08) проводилась обработка микросфокусированным ультразвуком с визуализацией (MFU-V) (800 линий обработки) нижней трети лица (с обеих сторон), всей области шеи и декольте (рисунок 1)
, а также правого нижнего квадранта живота.
Пункционная биопсия обработанной области живота (правый нижний квадрант живота) проводилась в рамках 1-го визита до начала процедуры, а также в рамках 3-го (M08) и 4-го визитов (M12) (рисунок 2)
.
В 4-й и 5-й визиты (M12 и M15, соответственно) филлер вводился подкожно в левую часть нижней трети лица, область шеи и декольте с левой стороны. В качестве контроля в правую часть нижней трети лица, область шеи и декольте с правой стороны вводился физиологический раствор.
Рисунок 1. Области обработки MFU-V
Рисунок 2. Область проведения пункционной биопсии
Введение препарата и обработка микросфокусированным ультразвуком проводились под местной анестезией. Крем наносился на 30–45 минут до начала лечения. Место введения препарата дезинфицировалось 0,05% раствором хлоргексидина диглюконата. Филлер вводился по методу профессора Юцковской.
Суть метода
Препарат вводился в виде раствора (разведение 0,9 % хлоридом натрия; соотношение 1:2, на 3 мл препарата 6 мл хлорида натрия) подкожно на границе дермы и гиподермы в линейно-ретроградной технике вдоль линий Лангера от периферии к центру и сверху вниз. Иглу вводили на всю длину (28G × 19 мм) со скосом вверх под минимальным углом к поверхности кожи.
Ссылки [ править ]
- Гидроксилапатит на Миндате
- Гидроксилапатит на Webmineral
- Энтони, Джон В .; Бидо, Ричард А .; Bladh, Kenneth W .; Николс, Монте С., ред. (2000). «Гидроксилапатит». Справочник по минералогии (PDF) . IV (арсенаты, фосфаты, ванадаты). Шантильи, Вирджиния, США: Минералогическое общество Америки. ISBN 978-0962209734. Архивировано (PDF) из оригинала 29.09.2018 . Проверено 29 августа 2010 .
- Сингх, Анамика; Тивари, Атул; Баджпай, Джая; Баджпай, Анил К. (2018-01-01), Тивари, Атул (ред.), «3 — Антимикробные покрытия на основе полимеров как потенциальные биоматериалы: от действия к применению» , Справочник по антимикробным покрытиям
, Elsevier, стр. 27– 61, DOI : 10.1016 / b978-0-12-811982-2.00003-2 , ISBN 978-0-12-811982-2, получено 18 ноября 2022 г. - Junqueira, Луис Карлос; Хосе Карнейро (2003). Фолтин, Джанет; Лебовиц, Харриет; Бойл, Питер Дж. (Ред.). Основы гистологии, текст и атлас (10-е изд.). Компании McGraw-Hill. п. 144 . ISBN 978-0-07-137829-1. Неорганическое вещество составляет около 50% от сухого веса кости … кристаллы имеют дефекты и не идентичны гидроксиапатиту, содержащемуся в минералах породы.
- Angervall, Леннарт; Бергер, Свен; Рёкерт, Ганс (2009). «Микрорадиографические и рентгеноструктурные исследования кальция в шишковидной железе и внутричерепных опухолях». Acta Pathologica et Microbiologica Scandinavica
.
44
(2): 113–119. DOI : 10.1111 / j.1699-0463.1958.tb01060.x . PMID 13594470 . - Ферраз, депутат; Monteiro, FJ; Мануэль, CM (2004). «Наночастицы гидроксиапатита: обзор методик получения». Журнал прикладных биоматериалов и биомеханики: JABB
.
2
(2): 74–80. PMID 20803440 . - Bouyer, E .; Гитцхофер, Ф .; Булос, Мичиган (2000). «Морфологическое исследование суспензии нанокристаллов гидроксиапатита». Журнал материаловедения: материалы в медицине
.
11
(8): 523–31. DOI : 10,1023 / A: 1008918110156 . PMID 15348004 . S2CID 35199514 . - ^ а б Рей, C .; Гребни, Ц .; Drouet, C .; Гроссин, Д. (2011). «1.111 — Биоактивная керамика: физическая химия». В Ducheyne, Пол (ред.). Комплексные биоматериалы
.
1
. Эльзевир. С. 187–281. DOI : 10.1016 / B978-0-08-055294-1.00178-1 . ISBN 978-0-08-055294-1. - Raynaud, S .; Чемпион, E .; Bernache-Assollant, D .; Томас, П. (2002). «Апатиты фосфата кальция с переменным атомным соотношением Ca / P I. Синтез, характеристика и термическая стабильность порошков». Биоматериалы
.
23
(4): 1065–72. DOI : 10.1016 / S0142-9612 (01) 00218-6 . PMID 11791909 . - Valletregi, М. (1997). «Синтез и характеристика кальциево-дефицитного апатита». Ионика твердого тела
. 101–103: 1279–1285. DOI : 10.1016 / S0167-2738 (97) 00213-0 . - Уивер, JC; Миллирон, ГВт; Miserez, A .; Evans-Lutterodt, K .; Herrera, S .; Gallana, I .; Mershon, WJ; Swanson, B .; Zavattieri, P .; Dimasi, E .; Кисаилус, Д. (2012). «Клуб Stomatopod Dactyl: грозный устойчивый к повреждениям биологический молот» . Наука
.
336
(6086): 1275–80. Bibcode : 2012Sci … 336.1275W . DOI : 10.1126 / science.1218764 . PMID 22679090 . S2CID 8509385 . Архивировано 13 сентября 2022 года . Проверено 2 декабря 2022 . - Таннер, KE (2012). «Маленький, но чрезвычайно прочный». Наука
.
336
(6086): 1237–8. Bibcode : 2012Sci … 336.1237T . DOI : 10.1126 / science.1222642 . PMID 22679085 . S2CID 206541609 . - ^ a b Хабиба, TU; Солсбери, HG (январь 2022 г.). «Биоматериалы, гидроксиапатит» . PMID 30020686 . Архивировано 28 марта 2022 года . Проверено 12 августа 2022 . Цитировать журнал требует |journal=( помощь )
- Карсия, CR; Scibek, JS (март 2013 г.). «Причинно-следственная связь и лечение кальцифицирующего тендинита и периартрита». Текущее мнение в ревматологии
.
25
(2): 204–9. DOI : 10,1097 / bor.0b013e32835d4e85 . PMID 23370373 . S2CID 36809845 . - «Архивная копия» . Архивировано 13 сентября 2022 года . Проверено 25 июля 2022 .CS1 maint: заархивированная копия как заголовок ( ссылка )
- «Архивная копия» . Архивировано 01 сентября 2022 года . Проверено 25 июля 2022 .CS1 maint: заархивированная копия как заголовок ( ссылка )
- Чжу, H .; и другие. (2018). «Наноструктурное понимание поведения растворения гидроксиапатита, легированного Sr». Журнал Европейского керамического общества
.
38
(16): 5554–5562. arXiv : 1910.10610 . DOI : 10.1016 / j.jeurceramsoc.2018.07.056 . S2CID 105932012 . - Вано, М .; Derchi, G .; Barone, A .; Pinna, R .; Usai, P .; Ковани, У (январь 2022 г.). «Снижение гиперчувствительности дентина с помощью зубной пасты с наногидроксиапатитом: двойное слепое рандомизированное контролируемое исследование». Клинические устные исследования
.
22
(1): 313–320. DOI : 10.1007 / s00784-017-2113-3 . ISSN 1432-6981 . PMID 28361171 . S2CID 24712149 . - ^ a b c d Штрауб, Д.А. (2007). «Добавки кальция в клинической практике: обзор форм, доз и показаний». Питание в клинической практике
.
22
(3): 286–96. DOI : 10.1177 / 0115426507022003286 . PMID 17507729 . - Ричардс, член парламента; Schulting, RJ; Хеджес, REM (2003). «Археология: резкий сдвиг в диете в начале неолита» (PDF) . Природа
.
425
(6956): 366. Bibcode : 2003Natur.425..366R . DOI : 10.1038 / 425366a . PMID 14508478 . S2CID 4366155 . Архивировано из оригинального (PDF) 07 марта 2011 года . Проверено 28 августа 2015 . - Бриттон, К .; Grimes, V .; Dau, J .; Ричардс, член парламента (2009). «Реконструкция миграций фауны с использованием внутризубных проб и анализов изотопов стронция и кислорода: пример современного карибу ( Rangifer tarandus granti
)».
Журнал археологической науки
.
36
(5): 1163–1172. DOI : 10.1016 / j.jas.2009.01.003 . - Дэниел Брайант, J .; Luz, B .; Froelich, PN (1994). «Изотопный состав кислорода ископаемого фосфата лошадиных зубов как отчет континентального палеоклимата». Палеогеография, палеоклиматология, палеоэкология
.
107
(3–4): 303–316. Bibcode : 1994PPP … 107..303D . DOI : 10.1016 / 0031-0182 (94) 90102-3 . - Ван Клинкен, GJ (1999). «Индикаторы качества костного коллагена для палеодиетических и радиоуглеродных измерений» . Журнал археологической науки
.
26
(6): 687–695. DOI : 10,1006 / jasc.1998.0385 . Архивировано 13 сентября 2022 года . Проверено 2 декабря 2022 . - ^ а б Санканнавар, Рави; Чаудхари, Санджив (2019). «Необходимый подход к смягчению последствий флюороза: внесение поправок в водный раствор кальция для подавления растворения гидроксиапатита при дефторировании» . Журнал экологического менеджмента
.
245
: 230–237. DOI : 10.1016 / j.jenvman.2019.05.088 . PMID 31154169 . Архивировано 18 мая 2022 года . Проверено 3 июня 2022 .
Лучшая паста без фтора: состав
Сначала пару слов хочется сказать про зубные пасты без фтора, которые мы условно отнесли к «устаревшему поколению». Дело в том, что они обладают намного более низкой ценой – в сравнении с качественными зубными пастами на основе настоящего медицинского нано-гидроксиапатита (nHAP). Выше мы уже говорили, что самая простая зубная паста без фтора – будет содержать одно из следующих соединений:
- глицерофосфат кальция,
- лактат кальция,
- пантотенат кальция,
- цитрат кальция,
- кальцис®.
Важно: наиболее качественные зубные пасты без фтора 1-го поколения будут содержать комбинацию – «глицерофосфат кальция + хлорид магния» (такая комбинация запатентована как Mineralin® и используется в зубных пастах ROCS). Дело в том, что ионы магния способны активизировать работу металлозависимых ферментов (кислой и щелочной фосфатаз), от которых зависит эффективность гидролиза глицерофосфата кальция – на активные ионы кальция и фосфаты.
В свою очередь зубные пасты SPLAT содержат запатентованное соединение – Кальцис®, представляющий из себя комплекс соединений кальция, полученных из яичной скорлупы. Он включает в себя водорастворимые дигидрофосфат, ацетат, лактат, сукцинат, цитрат и тартрат кальция. Тем не менее ни Mineralin®, ни Кальцис® даже близко не сделают зубную пасту без фтора – равной по противокариозной эффективности зубным пастам с фторидами или нано-гидроксиапатитом. Поэтому их лучше использовать только у детей в возрасте от 0 до 6 лет (причем только у тех – кто имеет самый низкий риск развития кариеса зубов).