Количество онкологических заболеваний неуклонно растëт во всём мире с каждым годом, а доля пациентов со злокачественными новообразованиями может достигать 1,4 % населения страны [1]. По прогнозам специалистов Всемирной организации здравоохранения, в ближайшие двадцать лет число случаев разных видов рака в мире возрастёт на 60 % [2]. На сегодняшний день в России проживают около 3,7 миллиона человек, больных каким-либо онкологическим заболеванием, что составляет примерно 2,6 тысячи случаев на 100 тысяч населения [3].
В настоящее время важным показателем эффективности лечения онкологических заболеваний является повышение качества жизни пациентов. Одной из его составляющих выступает своевременная стоматологическая помощь, направленная на сохранение здоровья и предупреждение болезней полости рта.
Как онкологические заболевания влияют на здоровье полости рта
Онкология развивается под воздействием как внешних, так и наследственных генетических факторов. Эта патология может поражать любую часть тела и не зависит от возраста пациента. Она начинается с изменений всего в одной клетке и приводит к серьëзным, часто фатальным последствиям для здоровья и жизни человека.
При развитии онкологического заболевания могут нарушаться функции поражëнных органов. Кроме того, эти патологии приводят к общему ухудшению состояния, снижению иммунитета, плохому настроению, депрессии, дисфункции пищеварения и анемии. Таким образом, злокачественные образования оказывают комплексное влияние на все системы и органы организма, в том числе и на состояние полости рта.
Что делать в случае нарушения памяти и внимания?
Прием химиотерапевтических лекарств вызывает нарушение работы нервной системы и проблемы с памятью. Если у вас возникли головокружения, потеря равновесия, спазмы и боль, ухудшение работы опорно-двигательного аппарата, сообщите об этих состояниях врачу.
Во время химиотерапии может нарушаться память и затормаживаться мышление. Иногда, возникает такое состояние, которое называется “хемо-мозг” — это нарушение когнитивных процессов, связанное с приемом препаратов, которые подавляют раковые клетки. Если у вас возникают нарушения внимания, запоминания, спутанность сознания, поговорите со своим врачом о преодолении этих неприятных симптомов.
Что делать?
- больше отдыхайте;
- составляйте план дел и действуйте по списку;
- просите о помощи своих близких;
- создайте напоминания в виде записок или пользуясь приложением в телефоне;
- делите большие дела на маленькие и конкретные задачи.
Как терапия онкологических заболеваний влияет на здоровье полости рта
Для лечения онкологических заболеваний применяются различные, часто интенсивные и агрессивные методы терапии. Для каждого вида рака, как правило, требуется свой особый режим лечения, который может сочетать хирургические методы с химиотерапией (лекарственные препараты) и лучевой терапией (направленное воздействие радиоактивного излучения). Все эти виды лечения направлены на подавление деления, развития и гибель раковых клеток. Однако часто они сопровождаются болезненными побочными эффектами, которые связаны с тем, что лучевая и химиотерапия губительно воздействуют и на нормальные клетки тканей, а также могут подавлять работу иммунной системы. При этом зачастую чем эффективнее метод лечения, тем выше степень его токсичности для пациента.
Кроме того, лучевая и химиотерапия часто имеют отдалённые последствия для здоровья, в том числе и стоматологического. Особенно важно учитывать это при лечении детей, перенёсших эти виды терапии онкологических заболеваний.
Среди побочных действий лучевой и химиотерапии, оказывающих непосредственное влияние на здоровье полости рта и еë лечение, наблюдаются:
- ухудшение общего состояния, слабость, тошнота;
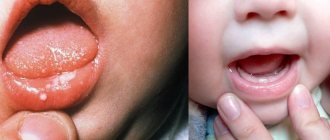
- заболевания слизистых оболочек, в том числе и слизистой оболочки полости рта, наиболее часто проявляющиеся как воспаления — стоматиты;
- снижение иммунитета и анемия, которые вызывают частые местные кровотечения.
Лечение злокачественных опухолей орофарингеальной области на современном этапе основывается на принципах мультидисциплинарного подхода, что позволяет уменьшить объем хирургических вмешательств, а в некоторых случаях даже избежать их [3]. Результаты применения комплексного подхода в лечении опухолей данной локализации, полученные большинством авторов, более эффективны, нежели результаты изолированного лучевого, химиотерапевтического или хирургического методов лечения [7].
Ведущие онкологические клиники имеют достаточный опыт комбинированного лечения опухолей орофарингеальной области, что позволяет оценивать отдаленные результаты и сравнивать их [4]. Однако для оценки эффективности лечения важным является изучение не только положительных, но и отрицательных эффектов, то есть осложнений и реакций. Одним из важнейших критериев эффективности любого метода лечения является снижение уровня отрицательных реакций и осложнений[1].
Материал и методы
Материалом настоящего исследования послужили данные проспективного, лонгитудинального изучения результатов лечения 586 больных со злокачественными новообразованиями орофарингеальной области. Все пациенты были разделены на 2 группы. В основную группу были включены 195 пациентов, группа сравнения была сформирована из 391 пациента. Отбор больных для исследования производился в соответствии со стандартными критериями включения и исключения. Критериями включения считали установленный диагноз злокачественного новообразования, планируемое комплексное противоопухолевое лечение, возраст от 18 до 84 лет, информированное добровольное согласие на участие в исследовании. Критериями исключения считались отказ больных от участия в исследовании, наличие тяжелой сопутствующей соматической патологии и психических заболеваний. При формировании групп для сравнительного анализа принимали во внимание индивидуальность подходов к лечению злокачественных новообразований в зависимости от локализации, стадии, гистологического варианта и особенностей лечебной программы (рис. 1).
Рисунок 1. Распределение больных по группам.
Результаты исследования
Анализ осложнений химиолучевого компонента комплексного лечения.
В зависимости от продолжительности времени после облучения и химиотерапии местные повреждения делятся на ранние и поздние. Ранние повреждения развиваются в процессе лучевой терапии или в ближайшие 3 мес после нее (крайний срок восстановления сублетального повреждения клеток). Поздними считают химиолучевые повреждения, развившиеся после указанного срока, чаще — через несколько лет [6].
В основе поздних химиолучевых повреждений лежат нарушения более радиорезистентных структур, являющиеся следствием постепенного накапливания изменений в мелких кровеносных и лимфатических сосудах, обусловливающих нарушение микроциркуляции и развитие гипоксии облученных тканей, что может впоследствии стать причиной фиброза и склероза [2, 4].
Из химиолучевых повреждений при проведении комплексного лечения рака орофарингеальной области мы в нашем исследовании наблюдали ксеростомию, лучевой кариес и лучевой остеорадионекроз.
Ксеростомию
называют отсроченным осложнением, однако на самом деле она начинает развиваться с первого дня лучевой терапии. Кроме того, это серьезное пожизненное осложнение, постоянно преследующее пациента и вызывающее ощущение сухой, жесткой слизистой оболочки. В первую неделю лучевой терапии наблюдается резкое снижение слюноотделения, которое за 2 нед лечения сокращается на 90%. При накоплении кумулятивной дозы облучения 40 Гр слюноотделение уменьшается на 95% по сравнению с первоначальным, и происходит необратимое поражение слюнных желез. Такое типичное уменьшение слюноотделения тесно связано с дозой облучения. При химиотерапии клиническая гипосаливация наблюдается только во время лечения и является обратимой.
Под нашим наблюдением находились 52 пациента из группы сравнения и 44 пациента из основной группы с ксеростомией, возникшей после химиолучевого лечения. Всем проводилась сиалометрия на момент госпитализации и после окончания курса химиолучевого лечения по «Методике сбора смешанной нестимулированной слюны в состоянии покоя». Средний показатель сиалометрии (общей нестимулированной слюны) на момент госпитализации составлял M=3,98±0,04. Все пациенты получили дозу облучения не менее 40 Гр. Повторные осмотры проведены нами по окончанию лучевого лечения и затем с 6-месячными перерывами.
Как правило, выделяются три степени ксеростомии, поэтому все пациенты были нами объединены и сгруппированы по степени выраженности симптомов (табл. 1).
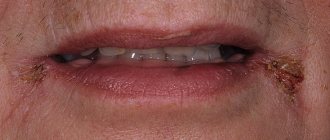
Безусловно, наиболее тяжелой для пациента (и для коррекции) является ксеростомия III степени. При нарушении функции слюнных желез III степени (функция слюнных желез полностью угнетена) больных беспокоят резкая сухость во рту, болезненные ощущения в слюнных железах, боль при еде, нарушение сна, речи. Отмечаются явления катарального глоссита, стоматита, слизистая оболочка ротовой полости сухая, гиперемирована, нередко с трещинами, эрозиями. Гипосаливация (сиалометрия — до 2 мл), повышенная вязкость, кислотность, пенистость слюны. Губы сухие, шелушатся, покрыты корками. Ксеростомия часто сопровождается множественным кариесом зубов (рис. 2, а).
Рисунок 2. Осложнения химиолучевой терапии. а — ксеростомия III степени, б — лучевой кариес.
Степень выраженности симптомов ксеростомии уменьшается с течением времени даже при отсутствии стоматологической помощи. Так, нами были обследованы пациенты группы сравнения (52 человека) непосредственно после завершения лучевой терапии и затем с 6-месячными перерывами. Динамика зависимости симптомов ксеростомии от времени, прошедшего с момента окончания химиолучевой терапии, представлена в табл. 2.
Так, симптомы, соответствующие III степени, наблюдались на протяжении 1,42±0,02 года и затем имели тенденцию к снижению, достигая своего минимума в среднем через 2,21±0,03 года.
При этом имеется прямая корреляционная зависимость степени выраженности ксеростомии от общей лучевой дозы (табл. 3).
Так, симптомы, соответствующие III степени ксеростомии, проявлялись при СОД=59 Гр. Предоперационный вариант лучевой терапии СОД=50 Гр приводил к возникновению ксеростомии I степени. Как видно из представленных выше данных, симптомы химиолучевой ксеростомии обратимы, что свидетельствует об отсутствии структурных поражений слюнных желез в процессе химиолучевого лечения. Однако восстановление количества отделяемой слюны — процесс достаточно длительный и тяжелый для пациента.
Лучевой кариес
(рис. 2, б) возникает после воздействия ионизирующего излучения на ткани зуба при лечении злокачественных образований головы и шеи. Клинические признаки постлучевого поражения зубов достаточно характерны. Обычно спустя 3—6 мес после лучевого воздействия эмаль зубов утрачивает характерный блеск, становится тусклой, серовато-блеклого цвета. Отмечается ломкость, стертость жевательной и вестибулярной поверхности зубов. На этом фоне появляются участки некроза, вначале локальные, а затем по типу циркулярного поражения зубов. Указанные поражения обычно темного цвета, заполненные рыхлой некротической массой, безболезненные. Отсутствие болевого симптома — характерная особенность радиационного поражения зубов, свидетельствующая о подавлении функции одонтобластов. Постепенно участки некроза расширяются и захватывают значительную часть зуба. Удаление некротических масс из очага поражения, как правило, безболезненное, поэтому требует особой осторожности. Если не применять радикальные вмешательства, то через 1—2 года окажутся пораженными более 96% зубов. Нами были обследованы пациенты через 2 года после завершения комплексного лечения опухолей орофарингеальной области. Все осмотренные пациенты получали лучевое лечение не менее 40 Гр. Лучевой кариес при осмотре диагностирован в 88% случаев (табл. 4, 5).
В табл. 6
представлена корреляционная зависимость развития лучевого кариеса в зависимости от полученной суммарной дозы (СОД).
Лучевой остеонекроз, радионекроз, некроз лучевой (radionecrosis)
— некроз ткани (чаще всего костной ткани или кожи), за счет угнетения ее регенераторной способности после проведенного курса противоопухолевой радиотерапии. Травма или хирургическое вмешательство (например, удаление зуба) после облучения могут усилить процесс радионекроза.
Лучевой остеонекроз представляет собой гибель костной ткани и является наиболее тяжелым последствием лучевой терапии онкологических заболеваний головы и шеи. В нашем случае 7 (9,3%) пациентов группы контроля обратились с жалобами на боли и длительное незаживление лунок после удаления зубов. Удаления были произведены в стоматологических учреждениях города в сроки от 7 до 12 мес после окончания лучевой терапии. Во всех случаях был выставлен диагноз «остеорадионекроз» (рис. 3).
Рисунок 3. Остеорадионекроз. Во всех случаях остеорадионекроз характеризовался длительным течением, с периодами обострения и отсутствием четко определяемых границ демаркации секвестра. Хирургическое вмешательство в основном было направлено на предупреждение развития абсцессов и флегмон ЧЛО. В одном случае течение радионекроза сочеталось с одновременным рецидивом опухоли.
Анализ осложнений хирургического компонента комплексного лечения.
Субтотальные и тотальные дефекты челюстей наиболее часто возникают после хирургического этапа комплексного лечения опухолей орофарингеальной области [8]. Хирургическое лечение злокачественных новообразований орофарингеальной области во многих ситуациях сопровождается резекцией значительного объема челюстных костей. При резекции верхней челюсти возникающие послеоперационные сообщения полости рта с полостью носа способствуют тяжелым функциональным расстройствам: нарушению акта жевания, глотания, дыхания, речи и слюноотделения [1]. Дефекты нижней челюсти приводят к нарушению жевания, речи и изменению эстетики внешнего вида. Рубцевание операционной полости ведет к резкому обезображиванию лица больного. Особенно выражен косметический изъян при комбинированной резекции челюстных костей с мягкими тканями лица, костными структурами глазницы, скуловой костью [5]. Все эти обстоятельства и неопределенность прогноза течения заболевания и жизни, нарушение жизненных планов и целей формируют у пациентов различные психогенные реакции, которые проявляются более чем у 90% больных [6]. В связи с этим лечение и реабилитация пациентов со злокачественными новообразованиями органов челюстно-лицевой области являются одной из наиболее сложных задач в онкологической клинике и требуют комплексного подхода [7, 8].
Нами были обследованы 73 пациента с дефектами челюстных костей: 54 (73,9%) случая — верхняя челюсть, 19 (26,1%) случаев — нижняя.
Дефекты верхней челюсти определялись по классификации D. Okay и соавт. (2001), разделяющей изъяны на 3 основных класса и 2 подкласса.
На нижней челюсти для систематизации возможных вариантов дефектов и деформаций и составления плана лечебной тактики мы использовали классификацию Л.В. Горбаневой, Б.К. Костур и В.А. Миняевой (1995), так как данная классификация не только рассматривает указанную патологию в зависимости от тяжести и степени выраженности дефекта или деформации, но и учитывает характер сращения или несращения отломков нижней челюсти, а также часто встречающиеся варианты дефектов нижней челюсти, образующихся после онкостоматологических операций в результате экзартикуляции половины или полного удаления нижней челюсти. Полученные результаты представлены в табл. 7.
К осложнениям хирургического лечения злокачественных новообразований орофарингеальной области также относятся: развитие контрактур, сужение ротовой щели (микростома), ограничение подвижности языка, губ и щек.
Контрактура
— ограничение подвижности сустава вследствие патологических изменений мягких тканей, костей или мышечных групп, функционально связанных с данным суставом.
Все контрактуры, возникающие после комплексного лечения опухолей орофарингеальной области, относятся к внесуставному типу. По степени раскрывания рта, внесуставные контрактуры делятся: на тяжелые (раскрывание рта до 1 см), средней тяжести (раскрывание рта на 1—2 см) и легкие (раскрывание рта на 2—3 см). Нами был обследован 391 пациент, получивший хирургическое лечение (в схеме комплексного лечения рака орофарингеальной области). Результаты оценки степени развития контрактур представлены в табл. 8.
Обсуждение
Главными стоматологическими осложнениями, возникающими после химиолучевой терапии, являются ксеростомия и лучевой кариес. Данные осложнения имеют высокую частоту встречаемости и, как правило, не проходят без оказания квалифицированной стоматологической помощи. Остеорадионекроз, являясь грозным осложнением лучевой терапии, к счастью имеет не столь широкое распространение. Основными осложнениями хирургического лечения, безусловно, являются дефекты челюстных костей и мягких тканей орофарингеальной области, сопровождающие каждое хирургическое вмешательство, а также возникающие послеоперационные внесуставные контрактуры. Все перечисленные осложнения имеют симптом взаимного отягощения, т.е. могут осложнять друг друга при проведении комплексной противоопухолевой терапии. Все развившиеся осложнения нуждаются в стоматологической коррекции. Стоматологическая помощь таким пациентам оказывается непосредственно после выписки из онкологического учреждения, далее в течение первого года стоматологический осмотр необходимо осуществлять каждые 3 мес, что будет сочетаться с контролем онкологическим. После первого года стоматологическое обследование выполняется каждые 3—6 мес в зависимости от индивидуальных факторов: уровня гигиены, степени развития ксеростомии, наличия восстанавливающих ортопедических конструкций.
Выводы
Проведенное нами исследование позволяет сделать следующие выводы.
1. Значительная часть нежелательных эффектов комплексного лечения злокачественных опухолей орофарингеальной области связана с химиолучевым компонентом и представлена в основном химиолучевыми реакциями. Из которых 34% приходится на клинически значимые радиомукозиты, вынуждающие делать перерывы в лечении и как следствие приводящие к снижению эффективности химиолучевого компонента.
2. Ксеростомия как осложнение химиолучевой терапии развивается с первого дня специализированной противоопухолевой терапии, причем в первую неделю наблюдается резкое снижение слюноотделения, которое при накоплении кумулятивной дозы облучения 40 Гр уменьшается до 95% по сравнению с первоначальным, однако степень выраженности симптомов ксеростомии уменьшается с течением времени даже при отсутствии стоматологической помощи.
3. Лучевой кариес, возникающий после воздействия ионизирующего излучения на ткани зуба, определяется до 88% случаев при облучении 40 Гр и до 96% случаев при облучении до 70 Гр, вызывая поражения твердых тканей зубов в сроки от 6 до 24 мес.
4. Хирургические осложнения в комплексном лечении рака орофарингеальной области составляют 20,2% и представляют собой дефекты лица и челюстных костей; нежелательные эффекты фотодинамической терапии представлены неспецифическими осложнениями в виде деформаций органов полости рта и возникновением сообщения с полостью носа и составляют 13,6%; коррекция всех указанных осложнений возможна только при взаимодействии хирургов-онкологов и стоматолога.
Лечение зубов при химиотерапии и лучевой терапии
Своевременная стоматологическая помощь способна значительно повысить качество жизни пациента с онкологическим заболеванием. Регулярные профилактические осмотры и лечение помогают избавиться от боли и воспалений, способствуют сохранению жевательной функции в полном объёме, предупреждают развитие патологических процессов в полости рта.
Однако при проведении лечения врач-стоматолог должен учитывать побочные действия получаемой пациентом лучевой и химиотерапии, а также влияние токсических реакций как на общее состояние пациента, так и на здоровье его полости рта.
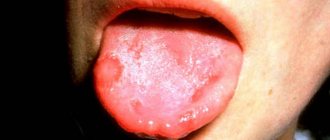
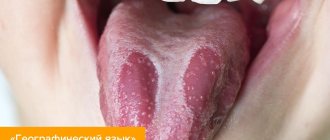
Наиболее часто на фоне лучевой и химиотерапии встречаются заболевания слизистой оболочки полости рта. Это стоматиты, кандидозы, папилломы языка, «географический язык» (воспалительное заболевание, проявляющееся в виде яркого рисунка на языке и вызывающее неприятные ощущения во рту) и другие виды глосситов (воспалений языка). Повышение риска развития подобных заболеваний связано с тем, что противоопухолевая терапия направлена в том числе на подавление иммунной функции организма.
Ещё одной группой заболеваний, риск развития которых повышает противоопухолевая терапия, являются заболевания пародонта. Они встречаются в 69,5 % случаев, при этом гингивит отмечается в 2 раза чаще, чем пародонтит [1].
Кроме того, пациенты, получающие лучевую и химиотерапию, могут жаловаться на неприятные ощущения во рту. Среди них:
- сухость во рту;
- образование язвочек и потëртостей;
- изменения вкуса;
- воспаления, отеки, кровоточивость дëсен и другие.
Выделяются в основном три проявления:
- язвенный;
- катаральный;
- афтозный.
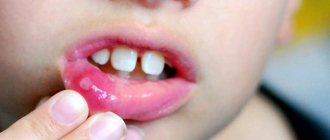
Изначально пациенты жалуются на появление покраснений и возникновение зуда, в последствие на пораженных участках наблюдаются язвочки, которые в дальнейшем лопаются, а на их месте образуются повреждения диаметром до 1 см.
Стоматит при химиотерапии пациенты могут выявить и самостоятельно, он сопровождается следующими признаками:
- повышается слюновыделение;
- наблюдает повышение температуры;
- снижение аппетита;
- болевые ощущения в ротовой полости.
Если вовремя не обратиться к специалистам, возможно возникновение кровоточащих язв. Несвоевременное вмешательство специалистов, может привести к осложнениям и распространению инфекции, что потребует более длительного лечения.
Особенности лечения заболеваний полости рта при лучевой и химиотерапии
Профилактический осмотр и консультацию врача-стоматолога пациенту важно пройти заблаговременно, до начала лучевой или химиотерапии. Это связано с тем, что обязательное обследование таких пациентов должно включать рентген- или томографическое исследование состояния костей челюстей и зубов, что позволяет исключить развитие в них патологического процесса.
Если пациенту необходимо хирургическое вмешательство в полости рта (например, удаление зуба) или протезирование зубов, стратегию лечения необходимо обсудить с лечащим врачом-онкологом и стоматологом. Как правило, хирургические вмешательства рекомендуется проводить за 2–3 недели до начала курса противоопухолевой терапии. Кроме того, до начала курса лечения необходимо выполнить санацию полости рта (вылечить кариозные полости), а также желательно провести курс реминерализации эмали.
Из-за повышенного риска кровотечения, плохой заживляемости ран, возможности развития воспаления или инфицирования при лечении стоматологических заболеваний у пациентов, получающих лучевую или химиотерапию, врачи-стоматологи должны соблюдать ряд предосторожностей.
- При осмотре полости рта врач должен обращать внимание на состояние дёсен и узнавать у пациента о случаях их воспаления или кровоточивости.
- Все вмешательства должны проходить с контролем анализа крови, в частности уровня лейкоцитов.
- Все вмешательства, начиная от местных инъекций анестетика до процедуры депульпирования канала, должны выполняться в максимально щадящей и бережной форме.
- Желательны консультации стоматолога с лечащим онкологом для корректной оценки состояния пациента.
- При необходимости перед лечением проводят курс антибиотиков, что позволяет снизить риск инфицирования.
Что делать при кровотечениях на фоне лечения химиопрепаратами?
Поражая клетки костного мозга, химиотерапия может снизить количество тромбоцитов в крови – клеток, которые отвечают за свертываемость крови. Если химиопрепараты повлияли на свертываемость крови, могут возникнуть синяки на теле, частые кровотечения из носа, небольшая сыпь на теле.
Что делать в случае угрозы кровотечений?
- осторожно обращайтесь с режущими предметами;
- избегайте слишком активной деятельности, в которой есть вероятность ушибов, порезов;
- используйте электробритву вместо станка;
- пользуйтесь мягкой зубной щеткой, исключите зубную нить;
- не допускайте возникновение запоров.
Осложнения развития зубов при лучевой и химиотерапии
Лечение злокачественных новообразований в детском возрасте значительно влияет на развитие зубов. При этом важно понимать, что развитие зубов — один из самых продолжительных процессов в человеческом организме, ведь полностью зубы формируются лишь к 21–22 годам [4]. Зачатки зубов содержат эмбриональные ткани, которые обладают свойствами интенсивно делиться и развиваться. Если ребëнок или подросток получает лучевую или химиотерапию, направленную на подавление активного роста клеток, это неизбежно сказывается и на развитии зубов. В частности, воздействие проявляется так:
- снижается устойчивость зубов к кариесогенным факторам;
- изменяется постоянство состава (гомеостаз) ротовой жидкости, в том числе еë очищающие свойства, снижается защитная функция и содержание микроэлементов и минеральных веществ, участвующих в реминерализации эмали и других;
- задерживается прорезывание зубов;
- увеличивается риск развития зубных аномалий, например недоразвития корней зуба, микродентии, нарушения формирования эмали, формирования полостей;
- погибают зачатки зубов, что ведёт к их отсутствию, при этом вероятность потери зубов особенно значительна при проведении химиотерапии в возрасте до 9 лет [4].
Детей, перенёсших химиотерапию, необходимо планово обследовать у стоматолога в раннем возрасте (оптимально в возрасте 6 лет, когда зачатки всех зубов в норме уже хорошо минерализованы и заметны на рентгенограммах, а для более старших детей — после завершения химиотерапии) для своевременной диагностики адентии и предупреждения вторичной деформации зубных дуг
Короленкова М. В., к. м. н., детский врач-стоматолог, Центральный научно-исследовательский институт стоматологии и челюстно-лицевой хирургии[4]
Причины стоматита после химиотерапии
Стоматит является частным случаем мукозита.
Мукозит — это воспалительная реакция слизистой оболочки верхних отделов желудочно-кишечного тракта от рта к животу (рот, губы, горло) и окружающих мягких тканей.
- Стоматит относится к воспалению во рту.
- Эзофагит относится к воспалению пищевода.
- Мукозит относится ко всем слизистым оболочкам.
Осложнение такого рода обусловлено применением определенных химиотерапевтических препаратов, индивидуальной реакцией, лучевой терапией и/или операцией. Эта реакция может прогрессировать в болезненные язвы и инфекции, мешая еде, разговору, вкусу, жеванию или глотанию и часто длится несколько дней.
Особенности гигиены полости рта у онкологических больных
На фоне побочного действия лучевой и химиотерапии онкологических заболеваний и развития возможных осложнений гигиена полости рта приобретает особое значение для пациентов. Она позволяет предотвратить развитие многих заболеваний и предупредить ухудшение состояния слизистой оболочки полости рта и зубов.
Пациенту важно особенно тщательно соблюдать все правила гигиены полости рта. В первую очередь гигиенические процедуры онкобольных должны включать:
- чистку зубов дважды в день, с использованием зубной щëтки с мягкой щетиной, которая поможет избежать травмирования дëсен, а также фторидсодержащей зубной пасты;
- осторожное и щадящее очищение межзубных промежутков зубной нитью (при кровоточивости дëсен нужно избегать болезненных участков);
- полоскание полости рта водой, которое поможет справиться с сухостью и предупредит раздражение слизистой оболочки полости рта.
На фоне противоопухолевой терапии не рекомендуется использовать ополаскиватели, содержащие спирт, так как он может вызывать неприятные и болезненные ощущения в полости рта и усиливать сухость слизистой оболочки. Кроме того, врач-стоматолог может рекомендовать использовать заменители слюны для устранения сухости, неприятных ощущений и профилактики кариеса и воспалений. Ещё одним средством, помогающим справиться с сухостью рта, является жевательная резинка, которая стимулирует выработку слюны. Пациентам, проходящим лучевую или химиотерапию, рекомендуется использовать жевательные резинки без сахара.
Кроме того, пациенту важно ежедневно самостоятельно осматривать полость рта (дëсны, язык и слизистую), обращая особое внимание на боль, кровоточивость, потёртости и ранки. Критически важными становятся и регулярные осмотры у специалиста-стоматолога, который сможет своевременно обнаружить возможную проблему и подобрать необходимое лечение. Помимо этого, очень важно посетить стоматолога до начала курса лучевой или химиотерапии.
Список источников
- Особенности стоматологического статуса у пациентов с онкологическими заболеваниями, Успенская О. А., Фадеева И. И. // Проблемы стоматологии. 2022. № 1. — URL: https://cyberleninka.ru/article/n/osobennosti-stomatologicheskogo-statusa-u-patsientov-s-onkologicheskimi-zabolevaniyami (дата обращения: 06.09.2020 г.).
- ВОЗ намечает меры по спасению 7 миллионов жизней от онкологических заболеваний // ВОЗ, Выпуск новостей 4 февраля 2020 г., Женева. — URL: https://www.who.int/ru/news-room/detail/04-02-2020-who-outlines-steps-to-save-7-million-lives-from-cancer (дата обращения: 06.09.2020 г.).
- Статистика онкологических заболеваний в РФ // Газета «Коммерсантъ» № 28 от 15.02.2020, стр. 2. — URL: https://www.kommersant.ru/doc/4258255 (дата обращения: 06.09.2020 г.).
- Короленкова М. В. Пороки развития зубов у детей после химиолучевого лечения // Вестн. РОНЦ им. Н. Н. Блохина РАМН. 2015. № 1. — URL: https://cyberleninka.ru/article/n/poroki-razvitiya-zubov-u-detey-posle-himioluchevogo-lecheniya (дата обращения: 06.09.2020 г.).
Консультация врача онколога, химиотерапевта в клинике «Витамед»
Для выявления причинно-следственных связей в процессе лечения заболевания может потребоваться помощь узкоспециализированных специалистов, так как недуг был спровоцирован химиотерапией.
Снять активное воздействие болезни на ротовую полость не сложно, необходимо выявить причины ее проявления, какими препаратами был спровоцирован стоматит при химиотерапии. Такой подход в лечении позволит избежать его проявления в будущем, так как он носит повторяющийся характер.
Вы можете прямо сейчас связаться с нами и записаться на прием к специалисту, который поможет в кратчайшие сроки побороть недуг.
9-20
Радиотерапевтическое лечение
Лучевая терапия при раке полости рта может быть дистанционной и контактной — брахитерапия, когда источник радиации находится не в ускорителе частиц, а непосредственно в организме пациента. Дистанционная лучевая терапия применяется в трех вариациях:
- Самостоятельно на первичный очаг и регионарные лимфоузлы при небольших размерах новообразования и невозможности хирургического лечения.
- Адъювантная лучевая терапия — проводится после оперативного лечения рака слизистой рта на его поздних, стадиях. Рекомендовано начать послеоперационную лучевую терапию в течение 6 недель после вмешательства.
- В составе адъювантной химиолучевой терапии при неполном удалении опухоли, прорастании капсулы лимфоузла и некоторых других неблагоприятных факторах на поздних стадиях процесса.
В ходе этой брахитерапии в опухоль устанавливаются специальные иглы — интрастаты, через которые по шлангам из контейнера подается радиоактивный кобальт или иридий (иногда другие элементы). Брахитерапия позволяет создать высокую дозу радиации непосредственно в опухоли, минимально затрагивая здоровые ткани, однако имеет несколько недостатков, которые ограничивают ее применение. К их числу относятся необходимость хирургического вмешательства и достаточно сложной подготовки. Процедура абсолютно противопоказана при инфильтрации опухоли в костную ткань и крупные сосуды, а также активная инфекция в месте установки интрастатов.
Методы профилактики
- Пройдите стоматологическое обследование. Посетите своего стоматолога, прежде чем начинать лечение рака, чтобы позаботиться о любых нерешенных проблемах с зубами, таких как заболевания десен, кариес или зубы, которые необходимо удалить. Любая боль или инфекции во рту только усугубятся, когда вы начнете лечение.
- Расскажите своему врачу, если уже были язвы во рту.
- В некоторых случаях лекарства могут предотвратить появление язв во время химиотерапии. Например, люди, которые страдают от стоматита из-за вируса простого герпеса, могут принимать противовирусные препараты для предотвращения таких осложнений во время терапии. Полоскание рта с использованием препарата дексаметазон может помочь избежать стоматита людям, получающим целевой препарат эверолимус.
- Ухаживайте за зубами. Привыкайте чистить зубы и полоскать рот несколько раз в день. Проверяйте этикетки на полосканиях для рта и избегайте спиртосодержащих продуктов.
- Прекратите курить. Если вы курите, бросьте. Курение во время лечения затруднит заживление полости рта.
- Соблюдайте диету, богатую фруктами и овощами. Вам понадобятся витамины и питательные вещества, чтобы помочь вашему организму бороться с инфекциями во время лечения.
Хирургическое лечение
В зависимости от места расположения и распространенности онкологического процесса, для хирургического лечения новообразований полости рта применяются различные операции, которые могут захватывать подлежащие костные ткани. Помимо этого иногда требуется также проведение реконструктивных вмешательств. На первой и второй стадии хирургическое лечение обычно назначается в самостоятельном варианте, на более поздних — сочетается с лучевой или химиолучевой терапией. В ходе операции, помимо вмешательства на первичном очаге, при необходимости и технической возможности проводится удаление пораженных регионарных лимфоузлов. Альтернативой операции на ранних стадиях может выступать схема, сочетающая дистанционную лучевую терапию с брахитерапией, которая подразумевает размещение источника радиоактивного излучения непосредственно в пораженные ткани.
Диетические рекомендации если установлена онкология
Следует ограничить потребление простых сахаров или заменить их аспартамом, ацесульфамом, сорбитом или ксилитом. Потребление продуктов с острыми, раздражающими слизистую оболочку специями должно быть ограничено. Предпочтительны пища теплая и с мягкими ароматами, с минимальными объемами специй. Избегайте фруктовых соков, в частности, кислых свежих фруктов, как из — за их слишком острого вкуса, так и из-за риска эрозии эмали. Уменьшить потребление кофе, чая и продуктов, вызывающих жажду (сухие бисквиты, крекеры, чипсы). В рационе должен быть исключен алкоголь в любых формах.
Следует иметь в виду, что поддержание сбалансированной диеты у пациентов, которые подвергаются химиотерапии и / или лучевой терапии вызывает специфические сложности.. Происходит изменение вкусовых ощущений, затруднение глотания, могут возникнуть тошнота и рвота. Кроме того, препараты, рекомендованные во время лечения оказывают неблагоприятное воздействие на некоторые пищевые ингредиенты, такие препараты,как неомицин уменьшают всасывание витаминов К и D, метотрексат, в целом, влияет на метаболизм витаминов, в частности, он реагирует с фолиевой кислотой и большинство препаратов могут привести к анорексии.
Доступные в аптеках пищевые композиции, в жидкой форме, содержащие набор витаминов, микроэлементов и аминокислот, обеспечивающих калорииность и питательные вещества, должны дополнять ежедневный рацион больных раком.
В случае развития стоматита наиболее эффективными препаратами являются кератопластики на масляной основе- аэкол, витамин А, Е. Но их заживляющее действие не высоко, данные препараты не более чем витамины.
Возникает необходимость в применении более продвинутых и эффективных специализированных препаратов.
EGF Эпидермальный фактор роста. Относится к группе полипептидов. Разрешены к применению в России только несколько его форм, в частности его предлагает московская фирма РЕПЛЕРИ в виде спрея для нанесения на слизистую оболочку либо кожу. Ранозаживляющее действие очень высокое, так же как и стоимость препарата. В медицине по прежнему применяется ограниченно, но в косметологии представлен очень широко, входит в состав многих косметических препаратов.
Palifermin – рекомбинантный человеческий фактор роста кератиноцитов, близкий к EGF препарат, сертифицированный и применяемый в Евросоюзе
РЕЗЮМЕ
Предотвращение стоматита у каждого пациента с онкологическим заболеванием должно быть частью терапии. Она имеет шансы на успех только за счет надлежащей мотивации самого пациента, его желания и самодисциплины. Безусловно, если у человека онкологическое заболевание, если во рту врач видит симптомы рака, то просьба заменить пломбу или провести протезирование вызывает у больного саркастическую усмешку. Помимо неприятных ощущений это еще и расходы, а лечение онкозаболеваний само по себе недешево.
И тут еще эти дантисты заводят старую надоевшую песню о необходимости иметь чистые зубы. Но следует напомнить, что стоматологические проблемы являются одним из провоцирующих факторов появления онкозаболеваний. Т.е. многие оказались у онколога именно из- за нелеченных зубов.
И в нашей практике мы встречали подобные случаи, В частности, вспоминается случай, когда у пациентки мы диагностировали онкозаболевание, развившееся под старым съемным протезом. Это была малигнизация участка слизистой оболочки под протезом с глубоким изъязвлением и реакцией региональных лимфатических узлов, классическая лейкоплакия. Наш диагноз в последующем подтвердился.
Но даже если заболевание все- же появилось, онкологи разработали эффективные схемы лечения и практика показала, что они добиваются успеха в большинстве случаев. Но сами онкологи признают, что полностью провести терапию не всегда возможно в силу появления осложнений, связанных с сопутствующими заболеваниями.
Любая терапия рака, да и всех опухолей основана на одном базовом принципе. Клетки опухоли находятся в стадии постоянного, лавинообразного деления и в этом состоянии у них есть одна уязвимость- они чувствительны к рентгеновским лучам и цитостатическим препаратам.
К сожалению, очень интенсивно обновляются и клетки эпителия желудочно кишечного тракта и полости рта. При терапии они так же становятся мишенями, хоть и в меньшей степени. Есть шанс их сохранить неповрежденными, исключив повреждающие факторы.
В заключении хотелось бы предостеречь людей от ошибок. Предлагаемые методы лечения и профилактики осложнений найдены путем долгих проб и ошибок. Медицина не всесильна и никогда не будет всесильной- даже если человечество научится лечить все известные болезни, им на смену просто придут новые и все повторится сначала.
Но есть в медицине прописные истины и законы, незыблемые аксиомы. Их исполнение служит выздоровлению. Другое дело, что болезнь может оказаться сильнее, так уж устроен этот мир.
Попытки заново придумать то, что уже создано и проверенно практикой предпринимаются постоянно, человек готов верить в сказку, ведь только сказка всегда дарит надежду.
Керосин с водкой, лечение рака содой, эксперименты с экскриментами — у здорового человека это вызывает усмешку. Но сознание меняется, если держит за горло грозный недуг. Если врач настраивает на тяжелый и трудный путь- а так хочется пройти все быстрее.
Если бы болезни вылечивались так легко, простым открытием метода.
В то- же время, если это только начало заболевания, а лечение проведено энергично и правильно, наступает полное выздоровление. Болезни ведь тоже не всесильны.
ГЛОССАРИЙ.
Эритема. Покраснение кожи или слизистых оболочек, вследствии гемостаза в капиллярах.
Эритроплазия (эритроплакии). Красные папулезные или макулярные поражения слизистой оболочки. Может произойти малигнизация.
Этиология. Изучение причин заболевания. С другой стороны, причина заболевания.
Струп. Структура, образующаяся на ткани, вызванная прижиганием или путем применения какого-либо деструктивного вещества.
Эстроген. Общий термин для естественного происхождения стероидных гормонов, содержащие ядро эстрон, эстриол estadiol, и т.д. выделяется из семенников, яичников и плаценты; стимулирует анаболические протеиновые действия и оказывает положительное влияние на баланс азота.
Экзогенных. Из-за внешних причин; не возникающие в организме.
Фибробласты. Клетки соединительной ткани; уплощенная, нерегулярно разветвленная клетка с большим овальным ядром, который отвечает, в частности, для производства и ремоделирование внеклеточного матрикса.
Фактор роста фибробластов. Семейство факторов роста с митогенных свойствами для фибробластов и мезодермальных типов клеток.
Фибронектин. Высокой молекулярной массой (450 кДа) гликопротеин, состоящие из двух соедененных дисульфидными связями полипептидов; функциональные домены молекулы обладают сродством к клеткам и компонентам внеклеточного матрикса; обнаружили на поверхности клеток, в соединительной ткани, в крови,
Фиброз. Волокнистое изменение слизистых оболочек, особенно десны, в результате хронического воспаления. Фиброзная десна может казаться внешне здоровой, маскируя основное заболевание.
Проточная цитометрия. Измерение физико- химических характеристик отдельных клеток, когда они движутся мимо оптических или электронных датчиков; может быть использован для обнаружения специфических клеток в смешанной популяции; используется для определения эффектов лекарств, гормонов, химических веществ.
Общий наркоз. Медикаментозное выключение сознания, в течение которого пациенты не отвечают на стиуляцию, даже болевую. Способность самостоятельно поддерживать функцию дыхания часто нарушается. Пациенты нуждаются в помощи в поддержании функции дыхательных путей.
Глюкокортикоиды. Группа кортикостероидов, секретируемых из коры надпочечников (такие как кортизол или дексаметазон), которые участвуют в обмене углеводов, белков, и жиров; которые регулируютк уровень гликогена в печени и уровень сахара в крови за счет изменения глюконеогенеза.
Гликозаминогликановые. Полисахаридая цепь, состоящая из гексозаминов чередующихся с другим углеводным остатком. компонент протеогликана.
ГРАФТ GRAFT. Любые аллотрансплантаты в виде гранул либо ксенотрансплантата гранулированный материал, помещенный с целью увеличения объема кости или регенерации костного дефекта.
Окраска по Граму. Способ классификации бактерий на две группы на основе окраски их клеточной стенки, после их окрашивания либо в фиолетовый (положительный) либо бледно-красный (отрицательный). Соответственно бактерии делятся на грамположительные и грамотрицательные
Факторы роста. Разнообразная группа полипептидов, которые играют важную роль в регуляции роста и развития различных органов.
Гуморальный иммунитет. Иммунный ответ опосредуется секрецией иммуноглобулинов (антител), полученных с помощью активированных В-клеток (плазматических клеток) против антигенов.
Гиперкератоз. Избыточное образование кератина эпителиальных клеток.
Гиперминерализация. Присутствие необычных количеств минеральных элементов в кальцинированной ткани.
Гиперкератоз. Ненормальное увеличение толщины эпителиального слоя (рогового слоя) эпителия.
Гиперостоз. Локализованный разрастание кости. Смотрите также экзостоз.
Гиперплазия. Увеличение размера структуры тканей в связи с увеличением числа клеток.
Гипофосфатазия. Гипофосфатазия: врожденное нарушение обмена веществ характеризуется дефицитом щелочной фосфатазы в сыворотке крови и костной ткани, что приводит к образованию дефектной кости и цемента.
Гипоплазия. Неполноценное или неполное развитие.
На ножке лоскут. Любой лоскут, который мобилизуется на новое место с использованием боковых надрезов, но сохраняет свою естественную связь у основания, чтобы сохранить его кровоснабжение.
Графт аутотрансплантат. Костная щебенка от донорского участка к участку- получателю в пределах того же индивидуума. Также известный как аутогенный трансплантат.
Блок графт. Graft. Аутогенной или аллогенный трансплантат кости в виде блока, используемого для увеличения костных участков .
Инородное тело. несвойственное вещество в тканях или полости тела.
Реакция на инородное тело. Гранулематозная реакция вокруг чужеродного материала в ткани или органе; часто характеризуется появлением гигантских клеткок. Это может проявляться как острое или хроническое воспаление десен и может привести к воспалению или гнойному поражению.
Уздечка. Складка слизистой оболочки ткани, которая прикрепляет губы и щеки к альвеолярной слизистой оболочки (и / или десной) и подстилающей надкостнице.
Фистула. Стома. Патологический канал, соединяющий полости двух полых органов или в полость органа с поверхностью тела.
Гидроксиапатит (ГА). Неорганическое соединение, СА (Р04) 6 (ОН) 2, найденный в матрицах костей и зубов, который обеспечивает жесткость этим структурам. Синтетические формы используются в медицине для замещения внутрикостных дефектов, а также для покрытия зубных имплантатов.
Кровоостанавливающий инструмент. Инструмент, который может быть использован, чтобы остановить кровотечение. Зажимы, клипсы.
Стадии рака
Стадирование, как и при других карциномах, производится по системе ТNM, где Т — распространение первичной опухоли, N — метастазы в регионарные лимфоузлы, М — отдаленные метастазы. Значение «0» после буквенного обозначения указывает на отсутствие признака.
| Стадия | ТNМ | Пояснение |
| I | Т1 N0 M0 | Т1 — локализованная опухоль размером менее 2 см |
| II | Т2 N0 M0 | Т2 — локализованная опухоль размером от 2 до 4см |
| III | Т3 N0 M0 T1-3 N1 M0 | Т3 — локализованная опухоль более 4см N1 — вовлечение одного узла со стороны поражения с его увеличением до 3 см. |
| IVA | Т1-3 N2 М0 Т4a N0-2 М0 | Т4a — прорастание в кости, гайморову пазуху, кожу, мышцы. N2 — вовлечение одного узла со стороны поражения с его увеличением от 3 до 6см, или в несколько узлов< 6см, или с противоположной стороны < 6см |
| IVB | Т4b N0-3 М0 Т0-4b N3 М0 | Т4b — рост в основание черепа, крылонебное пространство, основание черепа, сонную артерию. N3 — поражение узлов с их увеличением свыше 6 см |
| IVC | Любые Т и N при М1 | М1 — отдаленные метастазы |
При лечении на ранних стадиях прогноз 5-летней выживаемости составляет более 85% для первой стадии и 60-80% для второй. На более поздних стадиях этот показатель похуже (20 — 50%), а пациенту требуется комбинированное лечение.
Эффективность противорвотной терапии
Лечение таких осложнений после химиотерапии, как тошнота и рвота, может дать хороший эффект. Арсенал препаратов, которые обеспечивают профилактику и лечение тошноты и рвоты, очень большой. Комплексное их использование способно предотвратить появление этих симптомов в 90% случаев.
Полный контроль: отсутствие рвоты после введения противорвотных препаратов,
слабая тошнота
Частичный контроль: один эпизод рвоты или умеренная тошнота
Использование пробиотиков
Микрофлора полости рта также, как и флора кишечника делится на полезную, патогенную и условно-патогенную. Соответственно, для успешного лечения стоматита после химиотерапии, количество полезных бактерий должно быть достаточным, чтобы подавить вредные микроорганизмы, способные усугубить течение болезни. Пробиотики содержатся как в пищевых продуктах (кисломолочных, ферментированных), так и в специальных препаратах. Среди препаратов стоит выбирать жидкие, в которых находятся живые штаммы бактерий, способные быстро начать свою работу.
Посоветуйтесь с врачом, при некоторых видах и осложнениях рака пробиотики не рекомендованы к употреблению.
Факторы риска развития тошноты и рвоты
Существуют различные причины, предрасполагающие к появлению тошноты и рвоты. В первую очередь, это особенности используемого препарата или их комбинации.
Большое значение имеют индивидуальные особенности пациента:
- Возраст моложе 50 лет
- Женский пол
- Склонность к укачиванию в транспорте
- Присутствие утренней тошноты во время беременности
- Наличие тошноты и рвоты в течение предыдущего цикла химиотерапии
- Редкое употребление алкоголя
Наиболее тяжело химиотерапию переносят женщины и больные моложе 30 лет.