Автор статьи:
Солдатова Людмила Николаевна
Кандидат медицинских наук, профессор кафедры клинической стоматологии «Санкт-Петербургского медико-социального института», главный врач стоматологической клиники «Альфа-Дент» г. С-Петербург
Кандидоз или, иначе, молочница — это инфекционное заболевание, главной причиной которого является заражение грибками Candida. Эти грибки относятся к тому же виду, что и дрожжи, и входят в состав естественной микрофлоры у подавляющего большинства здоровых людей. Максимальная концентрация этих условно-патогенных микроорганизмов наблюдается в кишечнике, носоглотке, влагалище; некоторое количество грибков можно обнаружить и на поверхности кожи.
При нормальном, здоровом состоянии организма грибок не вызывает никаких неприятных симптомов. Однако при ослаблении иммунитета и появлении других провоцирующих факторов происходит активное размножение Candida, в результате чего и появляется дискомфорт, зуд, жжение и другие проявления молоцницы. Это заболевание может поражать различные ткани и органы; нередко встречается и кандидоз слизистой полости рта.
Чаще всего от этого заболевания страдают грудные дети: по данным статистики, до 20 процентов детей в возрасте до одного года хотя бы единожды переболели кандидозом. Около 10 процентов людей старше 60 также страдают от симптомов этой инфекции. У женщин он встречается чаще, чем у мужчин; очень часто признаки заболевания появляются у курильщиков. Существует и множество других факторов, способствующих развитию кандидоза во рту.
Причины кандидоза полости рта
Основная причина возникновения — это снижение иммунного статуса, в результате чего начинается бесконтрольное размножение микрофлоры. Сниженный иммунитет наблюдается у пожилых людей и у грудных детей, у пациентов, страдающих от ВИЧ, СПИД и других заболеваний, связанных с иммунодефицитом, у тех, кто регулярно подвергает организм чрезмерным нагрузкам, пренебрегает правилами здорового питания и нарушает режим работы и отдыха. К факторам риска можно отнести и такие причины, как:
- Употребление лекарственных препаратов.
Прием антибиотиков, иммуносупрессоров (препаратов, подавляющих иммунитет) и некоторых других лекарственных средств приводит к нарушению иммунитета и естественного баланса микрофлоры в организме. Похожее действие оказывают и оральные контрацептивы, влияющие на гормональный фон. - Беременность.
Во время вынашивания ребенка происходит резкое и значительное изменение гормонального фона, что может привести к всплеску активности патогенной и условно-патогенной микрофлоры. - Лучевая и химиотерапия.
Часто встречается у пациентов, проходящих медикаментозное и радиологическое лечение от раковых заболеваний. - Травмы слизистых оболочек.
Нарушение целостности слизистых оболочек приводит к утрате или ухудшению барьерной функции, в результате чего грибок попадает вглубь тканей, вызывает воспаление и другие симптомы. Особенно опасны мелкие, но постоянно повторяющиеся травмы — например, при ношении неправильно подобранных зубных протезов или брекетов. - Переутомление и стресс.
Длительное напряжение физических и психических сил приводит к ухудшению защитной функции организма. Аналогичные последствия вызывают переохлаждение или перегрев, регулярное недосыпание, недостаточное, чрезмерное или просто несбалансированное питание, злоупотребление алкоголем, никотином, наркотическими веществами. - Гипо- и авитаминоз.
Может быть вызван нехваткой питательных веществ, в частности — витаминов группы B, C. - Соматические заболевания.
Среди частых спутников кандидоза можно назвать туберкулез, дисбактериоз и другие патологии желудочно-кишечного тракта, болезни надпочечников и других желез внутренней секреции. Кандидоз является заразным заболеванием. Большое количество патогенных микроорганизмов передается при поцелуях и половых контактах, при пользовании общей посудой, полотенцами и другими предметами быта. Заражение также может произойти во время родов (вертикальная передача от матери к плоду). Кроме того, существует риск заражения при контактах с инфицированными домашними животными.
КАНДИДОЗ ПИЩЕВОДА
Кандидоз — инфекционное заболевание слизистых оболочек, кожи и внутренних органов, вызванное дрожжеподобными грибами рода Candida. Кандидоз пищевода (КП), являющийся проявлением висцерального кандидоза, занимает видное место среди инфекционных поражений пищевода. В последние годы прослеживается тенденция нарастания частоты КП, особенно у пациентов с нарушением иммунитета. Рост кандидозной инфекции в значительной степени обусловлен увеличением количества больных с ВИЧ-инфекцией, успехами в трансплантологии и иммуносупрессивной терапии, бесконтрольным использованием антибиотиков. КП встречается у 0,7-1,5% больных гастроэнтерологического профиля [5, 6].
Проблема тяжелых грибковых инфекций, вызываемых оппортунистическими патогенами, состоит в том, что они трудно поддаются лечению и могут приводить к летальному исходу. Было обнаружено, что смертность при инвазивных кандидозных инфекциях составляет 34% [16].
Этиопатогенез. Различные виды Candida представляют собой наиболее часто встречающийся пищеводный патоген, прежде всего это касается Candida albicans, иногда встречаются C. tropicalis, C. parapsilosis, C. glabrata, C. lusitania и C. krusei. Эти микроорганизмы являются нормальными компонентами оральной флоры, и их рост сдерживается бактериальными комменсалами. Заражение грибами типа Candida, которые широко распространены в окружающей среде, происходит эндогенным или экзогенным путем. Эндогенное заражение связано с активированием грибов-сапрофитов; экзогенное инфицирование может произойти при прямом контакте с носителями инфекции или из окружающей среды. Если организм хозяина не ослаблен, многие грибы не проявляют своих патогенных свойств. Исследования последних лет показали, что источником диссеминации грибов служит кишечник, а кандидоз полости рта, гениталий, пищевода является проявлением системного кандидоза. Вероятность развития системного поражения зависит как от свойств самого микроорганизма (их количества, вирулентности, генетической и видовой неоднородности популяции), так и от состояния макроорганизма, особенно его иммунной системы, алиментарного статуса и абдоминального кровотока [3, 17].
Благоприятные условия для развития инфекционного процесса создают различные нарушения физиологических, анатомических и иммунологических механизмов защиты организма. В качестве факторов, провоцирующих возникновение эзофагеального кандидоза, можно назвать использование антибиотиков, ингаляционных или инъекционных кортикостероидов, антацидную терапию или гипохлоргидрическое состояние, сахарный диабет, алкоголизм, последствия интоксикации, недоедание, пожилой возраст, нарушение моторики пищевода или пищеводную обструкцию, трансплантацию органов и костного мозга, энтеральное и особенно парентеральное питание и др. Ослабление иммунной системы может привести к возникновению кандидозной инфекции. При сахарном диабете повышенный уровень глюкозы в крови способствует росту грибов, так как гипергликемия ослабляет функцию гранулоцитов. Гипофункция паращитовидных желез и надпочечников приводит к нарушению кальциево-фосфорного обмена, что вызывает скрытую спазмофилию пищевода, тем самым снижая его местные защитные возможности [9]. Нарушения нутритивного статуса из-за недостатка белка в организме и низкой калорийности пищи влияют на состояние иммунной системы и создают предпосылки для развития кандидоза [3]. К факторам риска заболевания кандидозом относится снижение кислотности желудочного сока (рН 7,4 является оптимальной для роста грибов Candida, а при сдвиге рН до 4,5 рост грибов полностью угнетается) [3, 4, 7].
Патологические проявления КП разнообразны. Сначала пораженные участки пищевода имеют вид отдельных беловатых или желтоватых очажков, приподнятых над слизистой оболочкой. Позднее эти очажки могут сливаться, образуя плотные налеты с внедрением гриба в подслизистую оболочку или псевдомембранозные наложения с проникновением гриба в мышечную оболочку и сосуды [9]. Пленки, образующиеся на слизистой пищевода в особенно тяжелых случаях, могут почти полностью закрывать просвет пищевода. Налет состоит из слущенных эпителиальных клеток, которые смешиваются с грибками, клетками воспаления и бактериями. Микроскопическое исследование позволяет выявить равномерно окрашенные дрожжеподобные клетки и нити мицелия грибов Candida [9]. Истинное язвообразование наблюдается нечасто и в большинстве случаев отмечается у иммуносупрессированных больных с гранулоцитопенией [29]. Иногда возникает некроз стенки пищевода и развивается флегмонозное воспаление пищевода и средостения, что может стать одной из причин смерти больного [1].
Существует морфологическая классификация, согласно которой все случаи КП подразделяются на три группы в зависимости от степени тяжести процесса, то есть в зависимости от глубины поражения его стенки: 1-я группа — отдельные беловатые налеты с внедрением псевдомицелия гриба между эпителиальными клетками; 2-я группа — пленчатые налеты, сливающиеся между собой и образующие обширные поля, при этом нити псевдомицелия прорастают не только слизистую, но и подслизистую оболочку; 3-я группа — псевдомембранозные наложения, сочетающиеся с глубокими изменениями, при которых нити гриба глубоко проникают в толщу мышечной ткани [10].
Клинические проявления и осложнения. Симптомы заболевания практически отсутствуют у 25-30% пациентов, страдающих КП, особенно у иммунокомпетентных лиц. Тем не менее большинство пациентов предъявляют жалобы, связанные с поражением желудочно-кишечного тракта. Наиболее типичные клинические проявления КП — дисфагия и несколько реже одинофагия. Степень выраженности пищеводных симптомов колеблется от умеренного затруднения при глотании до резко выраженной боли, результатом чего являются неспособность принимать пищу и развитие вторичной дегидратации. При тяжелой одинофагии возможно наличие других причин или коинфекции, особенно у больных со СПИДом. Гораздо реже больные могут жаловаться на загрудинные боли, не связанные с глотанием, изжогу, тошноту, иногда рвоту с выделением пленок (псевдомембран), снижение аппетита и веса, появление жидкого стула со слизью (см. рисунок) [4, 9, 29].
| Симптомы кандиозного эзофагита (R. S. Orlando, 1996) |
При КП может быть полезно физикальное исследование. Приблизительно две трети пациентов со
СПИДом и пищеводным кандидозом имеют кандидозный стоматит. КП наблюдается у больных с хроническим слизисто-кожным кандидозом, который относится к тяжелым формам кандидозной инфекции и чаще наблюдается при дисфункции надпочечников и околощитовидных желез [29].
Осложнения пищеводного кандидоза наблюдаются редко. Эзофагеальное кровотечение может наблюдаться при тяжелом течении болезни, сопровождающемся образованием эрозий, язв, и ассоциироваться с коагулопатией; возможно развитие перфорации. Описана вторичная обструкция просвета мицетомой. Редко возникает некроз с развитием флегмонозного воспаления пищевода и средостения [1]. В тяжелых случаях специфический эзофагит может осложниться развитием кандидамикозного сепсиса [6].
Диагностика. Подозрение на пищеводный кандидоз должно возникнуть у любого больного при наличии факторов риска развития пищеводной инфекции и жалоб на дисфагию и одинофагию. Наличие кандидозного стоматита подтверждает этот диагноз, но при его отсутствии поражение пищевода также не исключается.
Рентгенография пищевода с использованием бария обычно применяется для начальной оценки перед проведением эндоскопии. Однако на ранних стадиях кандидозного эзофагита рентгенологическое исследование пищевода не имеет большого диагностического значения, так как оно отражает лишь неспецифические изменения, общие для всех эзофагитов [2]. Классическими рентгенологическими признаками острого эзофагита, вызванного Candida spp., являются линейные или неправильной формы дефекты наполнения с четкими краями. При тяжелом течении кандидозного эзофагита происходит слияние повреждений, из-за чего большие дефекты наполнения иногда образуют скопления в виде гроздьев винограда [2]. Пищевод при этом приобретает «косматый» («ворсистый») вид, симулируя ульцерацию [25]. Наличие больших, хорошо очерченных язв не является признаком кандидозного эзофагита. Могут наблюдаться нарушение моторики и сужение просвета пищевода за счет псевдомембран. Следует помнить о том, что нормальная рентгенограмма пищевода с использованием бария не исключает пищеводного кандидоза. Из-за тяжелой одинофагии больной не сможет выпить барий, что затрудняет рентгеногрфию пищевода [29].
Более информативным для диагностики кандидозного эзофагита считается рентгенологический метод двойного контрастирования, эффективность которого достигает 70% [26].
Цитологическая щетка и баллонный катетер используются для быстрой диагностики пищеводных инфекций без эндоскопии. Эти инструменты могут быть легко введены через носовые ходы или рот сквозь защитный зонд, который предотвращает контаминацию. Материал, полученный на защищенной щетке или баллонном катетере после того, как они будут изъяты из пищевода, оценивается цитологически и культурально. Методика с использованием защищенных щеток имеет чувствительность 88% и специфичность почти 100% [26].
Цитологический метод предполагает окраску мазков-отпечатков или осадка смыва с цитологической щетки в поисках активных форм Candida — почкующихся дрожжевых клеток, псевдомицелия и мицелия. Культуральный метод предполагает помещение исследуемого материала на обогащенную глюкозой среду Сабуро или другие среды, чтобы затем по характеру образующихся колоний судить об этиологии инфекционного процесса в пищеводе.
Эндоскопическое исследование пищевода — наиболее чувствительный и специфический метод диагностики пищеводного кандидоза. Эндоскопическая картина КП характеризуется чаще всего наличием легко снимающихся фибринозных рыхлых наложений белого или желтого цвета, под которыми обнаруживается легкоранимая и/или отечная слизистая. Реже наблюдаются катаральный и эрозивно-язвенный эзофагит [19]. Candida spp. редко вызывает истинное язвообразование. Наличие язвы при кандидозном эзофагите нередко служит признаком дополнительного патологического процесса в пищеводе [29]. Существуют различные эндоскопические классификации пищеводного кандидоза (табл. 1 и 2).
В ходе эндоскопии пораженные участки слизистой могут быть подвергнуты щеточной биопсии для цитологического исследования или биопсии для гистологической диагностики. Когда эндоскопически идентифицируются язвы, многократное проведение биопсии помогает исключить наличие сосуществующих патологических процессов. Цитологическое исследование материала, полученного с помощью браш-биопсии, имеет более высокую ступень чувствительности, чем гистологическое исследование образцов биопсии при умеренном поверхностном кандидозе, потому что микроорганизмы могут быть вымыты с поверхности ткани при обработке биопсийного материала [19]. В редких случаях позитивная цитология при наличии отрицательной гистологии указывает на то, что речь идет скорее о колонизации, чем об инфекции. При более тяжелом кандидозном поражении пищевода наибольшее диагностическое значение имеет гистологическое исследование биоптатов слизистой с использованием специальной окраски на нейтральные мукополисахариды по Шиффу PAS (ШИК-реакция) или по Gomori гексаметилентетрамином серебра. Только гистологическое исследование демонстрирует инвазию мицелия или псевдомицелия гриба в глубь ткани пищевода.
Кожное тестирование и серологические тесты малоинформативны для диагностики пищеводного кандидоза.
Лечение. Существует множество пероральных и внутривенных медикаментов, которые используются для лечения кандидозного эзофагита. Несмотря на относительно широкий выбор препаратов, лечение КП является актуальной проблемой, так как некоторые лекарственные средства недостаточно эффективны, другие имеют серьезные побочные эффекты; кроме того, в настоящее время отмечается рост резистентности к антигрибковым препаратам.
При лечении КП первоначально должна быть назначена пероральная терапия, внутривенное введение используется лишь в случае рефрактерного течения заболевания или если имеются противопоказания к пероральному использованию медикаментов. Больным с умеренной степенью тяжести заболевания и минимальным нарушением иммунитета необходим сокращенный курс терапии с использованием системных абсорбируемых лекарственных препаратов типа орального азола. Иммунокомпрометированных больных после трансплантации и больных СПИДом с КП лучше лечить более длинными курсами азола. У пациентов с гранулоцитопенией, когда имеется существенный риск диссеминации Candida инфекции, оправданно использование внутривенных препаратов системного действия (азолов, амфотерицина B) [29].
Арсенал современных противогрибковых средств достаточно широк. Для лечения пищеводного кандидоза используют антигрибковые препараты нескольких групп. Наиболее эффективны препараты из группы азола. Перорально используют невсасывающиеся азолы (клотримазол, миконазол); однако более эффективны препараты системного действия из этой группы (кетоконазол, флуконазол и итраконазол). Эти препараты, подобно другим из группы азола, изменяют проницаемость клеточной мембраны грибов посредством цитохром P450 (CYP)-зависимого вмешательства в биосинтез эргостерола, что приводит к повреждению грибной клетки и ее смерти. Новые триазолы (итраконазол и флуконазол) имеют большее аффинное подобие, чем имидазолы (миконазол и кетоконазол) для грибных CYP-энзимов [14]. Хотя другие средства, такие, как миконазол, клотримазол и нистатин, могут быть использованы для лечения кандидозного стоматита, а также для профилактики пищеводного поражения, эти лекарственные средства менее эффективны в качестве основной группы препаратов для терапии КП [24].
Клотримазол и миконазол — препараты имидазолового ряда. В настоящее время выпускаются клотримазол в таблетках и миконазол для перорального применения. Однако они не всасываются в желудочно-кишечном тракте. Эти препараты могут использоваться при легком кандидозном поражении пищевода у лиц без иммунодефицита.
Кетоконазол (низорал, ороназол) является производным имидазола и при ежедневном приеме в дозе от 200 до 400 мг дает хороший эффект в лечении пищеводного кандидоза. У больных СПИДом, которым обычно требуются более высокие дозы кетоконазола, дневная доза может быть увеличена, если не возникает тошноты, до максимальной (800 мг). Кетоконазол хорошо проникает в различные органы и ткани, но плохо — через гематоэнцефалический барьер. Препарат хорошо всасывается в желудочно-кишечном тракте, но для оптимального всасывания требуется кислая среда. При желудочной гипохлоргидрии и использовании антацидных средств его биодоступность уменьшается. Для улучшения всасывания кетоконазол следует принимать за 2 часа до приема противоязвенных препаратов. Приблизительно у 10-25% больных СПИДом наблюдается снижение желудочной кислотной секреции. Кетоконазол же может вызвать временную блокаду синтеза тестостерона и кортизола [6, 8, 29].
Итраконазол (споранокс) относится к группе триазолов, подобно кетоконазолу, назначается в дозе 200 мг в день. Дальнейшее увеличение дозы удлиняет период полураспада препарата и повышает его эффективность. Всасывание интраконазола уменьшается при снижении pH желудочного сока [23]. Кетоконазол и итраконазол метаболизируются в печени и выделяются с желчью. Период полураспада этих двух препаратов составляет от 7 до 10 часов и от 24 до 42 часов соответственно [14]. Коррекции дозы у больных с почечной недостаточностью не требуется.
Флуконазол (дифлюкан, дифлазон, форкан, флюкостат — отечественный флуконазол) представляет собой водорастворимый триазол и назначается в дозе 100 мг в день. Флуконазол — это препарат, всасывание которого не зависит от pH желудочного сока и который значительно более эффективен при лечении пищеводного кандидоза при СПИДе, чем кетоконазол (200 мг ежедневно) [21]. Флуконазол доступен для перорального и внутривенного применения. Он минимально метаболизируется и выделяется неизмененным с мочой. Флуконазол отличается высоким тканевым тропизмом и не влияет на синтез андрогенов, хорошо проникает через гематоэнцефалический барьер. В отличие от кетоконазола и интраконазола он хорошо растворим в воде и минимально связывается белком. Препарат обладает длительным периодом полураспада (приблизительно 30 часов, если не нарушена функция почек, а наличие пищи или гипохлоргидрия не изменяют всасывание), что позволяет принимать его один раз в сутки. Показано, что введение флуконазола улучшает иммунные показатели по Т- и В-системам [18]. И флуконазол, и итраконазол можно принимать перорально в виде растворов. Эти формы могут быть более эффективны, чем таблетки, потому как усиливают локальный эффект и улучшают всасывание.
Неблагоприятные воздействия кетоконазола, флуконазола и итраконазола прежде всего зависят от дозировки и проявляются в виде тошноты, гепатотоксичности, замедления продукции стероидов и метаболизма циклоспорина [14]. В редких случаях кетоконазол может вызывать фатальный гепатит [12]. Незначительное увеличение аминотрансфераз — общий побочный эффект для всех трех препаратов, однако это не должно служить оправданием для их отмены. Влияние на стероидогенез наиболее выражено у кетоконазола. Обратимое замедление гонадального и надпочечного синтеза стероидов под воздействием кетоконазола может наблюдаться, когда доза превышает 400 мг в сутки [27]. В рекомендуемых дозах флуконазол и итраконазол не влияют на стероидогенез. В результате воздействия на печеночные микросомальные ферменты все три азола ингибируют метаболизм циклоспорина, что приводит к увеличению уровня циклоспорина в крови; этот эффект наиболее ярко выражен у кетоконазола [14].
Другая основная группа противогрибковых средств — антибиотики полиены, представленные амфотерицином и нистатином. Эти препараты необратимо связываются со стеролами в грибковых клеточных мембранах, тем самым изменяя свойства проницаемости мембраны, нарушая ее барьерную функцию и вызывая клеточную смерть. Нистатин (антикандин, микостатин, фунгицидин) практически не всасывается в желудочно-кишечном тракте. Он используется для лечения кандидозного стоматита, но менее эффективен при поражении пищевода. Кроме того, эффективность, безопасность и легкость применения производных азола позволяют рассматривать нистатин в качестве средства терапии второго ряда. Амфотерицин В (амфостат, фунгизон) — единственный полиеновый антибиотик для парентерального введения. Он не всасывается в желудочно-кишечном тракте, применяется внутривенно капельно, хорошо проникает в различные органы и ткани, выделяется из организма почками. Период полувыведения составляет 24-48 часов, однако при систематическом применении может возрастать до 15 дней вследствие кумуляции в тканях [8]. Хотя амфотерицин B является наиболее эффективным препаратом, использующимся для лечения системных микозов, но из-за серьезных побочных эффектов его применение в лечении КП ограничено. Среди побочных эффектов амфотерицина можно выделить нейротоксичность, гематоксичность, нефротоксичность, местно-раздражающее действие (флебиты), аллергические реакции, диспептические расстройства, лихорадку и др. [8]. Наиболее неблагоприятным побочным эффектом, возникающим вследствие длительного использования амфотерицина, является нефротоксичность, которая обычно обратима. Этот препарат теперь доступен в виде раствора для перорального применения и пастилок. У больных с КП, которые резистентны к лечению флуконазолом или другими азолами, эффективными могут быть низкие дозы амфотерицина B, вводимого внутривенно (от 10 до 20 мг в день). Общая доза препарата для лечения пищеводного кандидоза составляет от 100 до 200 мг [29].
Флуцитозин — препарат с узким спектром противогрибковой активности, который действует благодаря вмешательству в трансляцию РНК. Он включается в клетки гриба, где превращается в 5-фторурацил и ингибирует тимидилат-синтетазу. Этот пероральный препарат, который назначается в дозе от 50 до 150 мг/кг в день каждые 6 часов, может быть использован в комбинации с амфотерицином B, но он не должен применяться в качестве монотерапии, потому что грибы быстро становятся к нему резистентными. Кроме того, монотерапия флуцитозином оказывается лишь умеренно эффективной [12].
Новейшим классом противогрибковых препаратов являются кандины, вмешивающиеся в синтез грибковой стенки. Они эффективны в отношении большинства видов Candida, в том числе C. krusei. Первые исследования показали, что капсофунгин, представляющий эту группу препаратов, оказался столь же эффективен при КП, как и амфотерицин В [16].
При лечении больных КП следует учитывать наличие резистентности, которая из-за широкого применения азолов в настоящее время значительно возросла. При развитии резистентности часто бывает полезно увеличить дозу азола. Если этого оказывается недостаточно, переходят на другой препарат из этой группы или используют пероральный раствор итраконазола [13], который нужно назначать в более высоких дозах из-за часто наблюдающейся перекрестной резистентности. Когда высокой дозы (то есть 400 мг ежедневно) флуконазола недостаточно, переходят на внутривенное введение амфотерицина B, при этом результат достигается в 90% случаев. Резистентность к амфотерицину наблюдается редко [29].
В табл. 3 представлено лечение кандидозного эзофагита в зависимости от функции лимфоцитов и гранулоцитов.
При лечении кандидозного эзофагита у больных СПИДом препаратами первого ряда являются кетоконазол и флюконазол, причем предпочтение следует отдавать флюконазолу. Из-за лучшей переносимости он прежде всего показан пациентам, находящимся на поздней стадии болезни, которые имеют много сопутствующих заболеваний. При нарушении глотания могут применяться парентеральные формы флуконазола. При неэффективности препаратов первого ряда используют лекарственные средства из группы резерва (амфотерицин В, итраконазол), которые более токсичные и/или более дорогие. Этиотропная терапия кандидоза пищевода, кроме основного курса лечения, требует проведения поддерживающего лечения, которое может быть пожизненным (табл. 4) [4].
Лечение кандидоза на фоне тяжелого иммунодефицита и лейкопении — задача сложная. Наряду с антигрибковой терапией актуально восстановление пула нейтрофильных лейкоцитов и их функциональной активности, так как нейтрофильные лейкоциты являются одним из основных звеньев механизма защиты от Candida spp. Предлагается в качестве дополнительного средства при лечении кандидозной инфекции на фоне нейтропении использовать гранулоцитарный колониестимулирующий фактор, который сокращает дефицит миелопероксидазы в нейтрофильных лейкоцитах и усиливает их кислородозависимую антикандидозную активность [7]. Получен хороший эффект от эндоскопического введения больным КП концентрата гранулоцитов и высокоинтенсивного импульсного лазерного излучения, что улучшает иммунные функции [5].
Таким образом, для достижения успеха у больных с тяжелыми грибковыми инфекциями, в том числе с кандидозом, целесообразен комплексный подход к диагностике и лечению. Повышению выживаемости будет способствовать оперативная диагностика с последующими подбором эффективной специфической противогрибковой терапии и проведением лечебных мероприятий, направленных на повышение числа гранулоцитов и стимуляцию фагоцитоза [16].
По вопросам литературы обращайтесь в редакцию
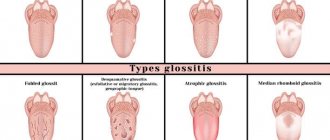
Виды заболевания
Клиническая картина кандидоза полости рта классифицируется:
- На клинико-морфологическую.
- По течению.
- По локализации.
Клинико-морфологическая делится на:
- Гиперпластическую.
- Эрозивно-язвенную.
- Псевдомембранозную.
- Атрофическую.
Клиническая картина, классифицируемая по течению, делится на:
- Хроничекую.
- Острую.
По локализации:
- Хейлит.
- Гингивит.
- Глоссит.
- Стоматит.
- Тонзиллит и др.
Исходя из клинической картины, кандидоз полости рта бывает нескольких видов:
- Хронический гиперпластический.
- Кандидозная заеда.
- Хронический атрофический.
- Острый псевдомембранозный.
- Хронический псевдомембранозный.
- Острый атрофический.
Симптомы
Поражение слизистой полости рта грибком Candida может принимать различные формы, каждая из которых имеет собственные особенности симптоматики. Наиболее распространены такие формы болезни, как кандидозный ангулит, глоссит, хейлит, стоматит. Встречается как острая, так и хроническая формы заболевания.
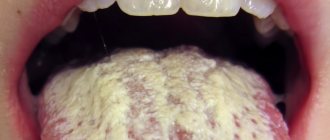
- Псевдомембранозный острый кандидоз является самой распространенной формой и чаще всего встречается у младенцев и пожилых людей. Для этой формы характерно появление выраженного отека, гиперемии (покраснения) слизистых оболочек. Кроме того, на поверхности губ, неба, спинке языка и внутренней стороны щек образуется характерный беловатый налет. Если налет соскрести, поверхность слизистой под ним будет мацерированной (размягченной) или изъязвленной, кровоточащей. При этом у пациентов возникают жалобы на болезненность, жжение или зуд во рту; прием пищи в значительной степени затрудняется. Очень часто процесс распространяется на пищевод, глотку.
- Острый атрофический кандидоз слизистой оболочки полости рта обычно развивается из-за отсутствия адекватного лечения. Верхняя часть слизистых (эпителий) при этом слущивается, слизистая становится тонкой, красной или напротив — отечной. Яркий красный цвет приобретает и язык пациента, уголки губ; сосочки на языке атрофируются, сглаживаются. Налет при этом отсутствует или обнаруживается лишь в труднодоступных местах.
- Гиперпластический хронический кандидоз характеризуется образованием большого числа папул и бляшек неправильной или округлой формы. Они располагаются близко друг к другу на слизистой языка и щек и нередко спаиваются, срастаются. Вокруг каждого такого образования имеется тонкий ободок покрасневшей, воспаленной ткани. Соскоблить или удалить иным образом такую бляшку затруднительно. Полость рта при этом становится сухой и шероховатой; при жевании, говорении и даже в покое у пациентов обнаруживается значительный дискомфорт и болезненность. Следует отметить, что это заболевание чаще всего поражает мужчин старше 30 лет.
Главной причиной хронического атрофического типа является постоянное травмирование слизистых оболочек, например — из-за ношения протеза. Симптомы заболевания локализуются в области поражения. Возникает покраснение слизистой (часто — по контуру поражения), образуется налет, возникают боль и жжение, оболочки становятся сухими.
Как проявляется заболевание у детей?
У детей болезнь протекает в острой форме и сопровождается появлением покраснения и отеков на слизистой оболочке полости рта. Ребенок плохо спит, у него может отсутствовать аппетит, появляется плаксивость.
Болезнь у детей может возникнуть по следующим причинам:
- Ослабление иммунитета.
- Заражение при кормлении грудью.
- Передача грибка во время родов.
- Заражение через бытовые предметы.
Если заболевание своевременно не диагностируется и не лечится, в скором времени у ребенка во рту появляется белесый налет, напоминающий творог, а в запущенной стадии возникают язвы, которые сопровождаются кровоточивостью и вызывают сильную боль у малышей.
Условия эффективного лечения
Эффективное лечение молочницы во рту предусматривает устранение основной причины. Очень важно санировать полость рта: вылечить зубы, разрушенные кариесом, удалить нежизнеспособные зубы и корни, которые уже не подлежат восстановлению. Это хронические очаги воспаления, поэтому одновременная санация сократит время лечения. Также следует удалить зубной камень и налет. Особенно это касается случаев кандидозного стоматита, связанных с травмированием десен острыми краями твердых зубных отложений.
Пациенты со съемными протезами должны быть повторно обучены гигиене и дезинфекции ортопедических конструкций. Если время пользования протезом подходит к концу, важно своевременно заменить его. Лечение кандидоза будет бесполезным, если человек будет пользоваться протезом неправильно и снова создавать в полости рта условия для размножения грибов.
Замене подлежат и неподходящие коронки, мостовидные протезы и другие конструкции. Также важно устранить сколы эмали, которые становятся источником травм для десен, слизистых оболочек щек и языка.
Курильщики должны по возможности сократить эпизоды курения или отказаться от вредной привычки. Если болезнь развилась на фоне приема кортикостероидов, важно разъяснить правила лечения: следует полоскать полость рта большим количеством теплой воды после распыления препарата.
При лечении кандидоза полости рта, развившемся на фоне антибактериальной терапии, следует принимать меры по восстановлению нормальной микрофлоры кишечника и полости рта. Может потребоваться консультация другого специалиста узкого профиля или терапевта: потребуется прием пробиотиков и пребиотиков.
Для всех пациентов, которые лечат кандидоз, действует несколько общих рекомендаций:
- соблюдение гигиены полости рта;
- отказ от пищи, богатой углеводами;
- отказ от сладких напитков.
Необходимо исключить из рациона пищу, которая может раздражать слизистую: блюда, приготовленные с уксусом, маринады, острые, перченые продукты, копчености, кислые фрукты и ягоды. Также нельзя есть кондитерские изделия, выпечку на дрожжах, сахар. Лучше отдавать предпочтение теплым блюдам. Соблюдать такой режим питания нужно еще в течение 1,5−2 месяцев после выздоровления.
В ряде случаев целесообразно использовать зубные пасты с оксидазой глюкозы, лизоцимом, лактоферрином. Они способствуют улучшению защитных сил слизистой оболочки полости рта и могут быть частью комплексной профилактики развития воспалений. Выбор зубной пасты нужно согласовать с врачом, он порекомендует оптимальное средство, а также расскажет о том, какая щетка подойдет.
Диагностика
Для точной постановки диагноза используют сочетание нескольких методов — от простого осмотра и опроса пациента на предмет жалоб до лабораторных, таких как посев, микроскопическое исследование биоматериала, анализ степени обсеменения ротовой полости грибковым мицелием.
Кандидоз рта сопровождается целым рядом характерных наружных признаков, в частности — образованием налета, запахом изо рта, изъязвлением и гиперемией слизистых. Однако лабораторные методы позволяют точно определить тип возбудителя и исключить возможность наличия вторичной инфекции, что может повлиять на характер и длительность лечения.
Дифференциальная диагностика применяется для отделения случаев кандидоза от заболевания афтозным стоматитом, лейкоплакией, красным лишаем, стрептококковой заедой и другими инфекционными патологиями полости рта.
Основы лечебного рациона
Сбалансированное питание при кандидозе должно включать в себя такие компоненты, как:
- Нежирные сорта рыбы и мяса;
- Овощи;
- Куриные яйца;
- Гречка.
- Продукты с антигрибковым эффектом.
Комплексное лечение наиболее эффективно при правильном питании. Эти ингредиенты должны составлять основу рациона. Немаловажное значение специалисты придают количеству приемов пищи, а также температуре готового блюда. Идеальным решением станет отказ от соли и различных приправ.
Они раздражают слизистую оболочку ротовой полости, создавая благоприятную среду для роста патогенной микрофлоры. Приготовленные на пару или отварные продукты оказывают щадящее воздействие на ротовую полость.
Как лечить кандидоз полости рта?
Лечение проводится с применением местных и общих, специфических и симптоматических средств. Среди основных задач терапии можно назвать устранение очагов инфекции в ротовой полости (санацию), лечение заболеваний, которые сопутствуют кандидозу и являются факторами риска, стимуляцию защитных сил организма. Общая длительность лечения обычно составляет не менее 7-10 дней.
В качестве средств местной терапии используются полоскания — с использованием растворов борной кислоты, соды, тетрабората натрия. Для более длительного и эффективного воздействия такие средства можно применять в виде аппликаций — смочив раствором ватный тампон или бинт.
Нистатин при кандидозе полости рта используется для борьбы с основной причиной заболевания — грибковой инфекцией. Лечение кандидоза во рту также может включать в себя применение других антимикотических (противогрибковых) препаратов — например, левориновой мази. Наилучший эффект достигается при использовании нескольких препаратов, чередовании их в течение нескольких дней.
Противогрибковые препараты назначают и для системной терапии — в этом случае внутрь принимают такие лекарства от кандидоза полости рта и других инфекций, как ламизил, дифлюкан, леварин, низорал и др. В наиболее тяжелых случаях заболевания в схему терапии включают прием иммуномодулирующих препаратов, а также использование других средств, оказывающих стимулирующее воздействие на иммунитет и способствующих укреплению собственных защитных сил организма.
Не менее важной задачей является защита от дополнительных грибковых и бактериальных инфекций, которые могут присоединиться к заражению грибком Candida и осложнить течение болезни. С этой целью проводят полоскания антисептическими растворами — фукорцином, йодинолом и другими.
В качестве альтернативного средства можно использовать антисептический ополаскиватель для полости рта АСЕПТА, содержащий активные компоненты хлоргексидин и бензидамин. Оба этих вещества обладают широким противомикробным действием. Регулярное применение ополаскивателей АСЕПТА также оказывает выраженный противовоспалительный эффект и помогает не только устранить неприятные симптомы, но и снизить риск развития осложнений.
Особенности лечения
Основу лечения составляют системные и местные противогрибковые препараты. Сегодня они широко представлены на фармацевтическом рынке, но важно знать о том, что ежегодно уровень резистентности грибов Candida растет к основным средствам. Например, к таким препаратам, как «Флуконазол» устойчивость почти полная. Раньше это средство использовалось почти во всех случаях заболевания, но сегодня врачи вынуждены пересмотреть стандартные схемы терапии.
Лечение молочницы во рту у взрослых подбирается индивидуально. Выбор системного противогрибкового средства основывается на виде возбудителя, состоянии пациента и индивидуальных особенностей его здоровья. Существуют средства, к которым у инфекции минимальная устойчивость. Врач может назначит препараты на основе нистатина, производных имидазола и др.
Дополнительно обязательно используются местные средства:
- растворы для полоскания полости рта;
- гели и суспензии для аппликаций на пораженные участки;
- местные таблетки и пастилки для рассасывания;
- растворы для орошения и аэрозоли;
- мази для закладывания в полости рта на ватно-марлевом тампоне и др.
Специалист может назначить аптечные антисептики или слабые солевые растворы для полоскания. Обычно используют растворы на основе йода, хлоргексидина, калия перманганата, генцианвиолета, натрия тетраборат в глицерине. Некоторые таблетки врач может порекомендовать закладывать за щеку.
Профилактика заболевания
Профилактические мероприятия направлены на улучшение состояния микрофлоры. К ним относят:
- Правильную гигиену полости рта.
- Продуманный рацион питания с высоким количеством белковых продуктов и сниженным употреблением пищи, содержащей глюкозу.
- Отказ от курения и спиртных напитков.
- Своевременный осмотр у лечащего стоматолога для профилактики, диагностики и лечения болезни.
- Отказ от приема медицинских препаратов, таких как антибиотики, без предварительной консультации с врачом.
- Если у пациента имеются зубные протезы, то одной из мер профилактики будет их регулярная обработка в специальном растворе.
Источники:
- Роль противовоспалительного ополаскивателя в лечении заболеваний пародонта (Л.Ю. Орехова, А.А. Леонтьев, С.Б. Улитовский) Л.Ю. ОРЕХОВА, д.м.н., проф., завкафедрой; А.А. ЛЕОНТЬЕВ, врач-стоматолог; С.Б. УЛИТОВСКИЙ, д.м.н., проф. Кафедра терапевтической стоматологии СПб ГМУ им. акад. И. П. Павлова
- Отчет о клинических испытаниях по определению/подтверждению профилактических свойств средств индивидуальной гигиены полости рта выпускаемых серийно: ополаскиватель для полости рта «АСЕПТА PARODONTAL» — Раствор для ирригатора». д.м.н. профессор, заслуженный врач РФ, зав. кафедрой Профилактической стоматологии С.Б. Улитовский, врач-исследователь А.А. Леонтьев Первый Санкт-Петербургский государственный медицинский университет имени академика И.П. Павлова, кафедра профилактической стоматологии.
- Изучение клинической эффективности лечебно-профилактических средств линии «Асепта» при лечении воспалительных заболеваний пародонта (А.И.Грудянов, И.Ю. Александровская, В.Ю. Корзунина) А.И. ГРУДЯНОВ, д.м.н., проф., руководитель отделения И.Ю. АЛЕКСАНДРОВСКАЯ, к.м.н. В.Ю. КОРЗУНИНА, асп. Отделение пародонтологии ЦНИИС и ЧЛХ Росмедтехнологий, г. Москва