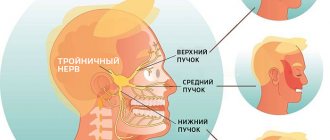
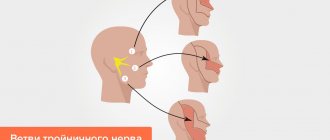
Нижняя челюсть подвергается травматическому повреждению намного чаще других костей лицевой части черепа. Хотя она и относится к наиболее прочным костям, ее подвижность и выступающее положение предопределяет подверженность переломам. До 85% всех повреждений костей лица приходится на переломы нижней челюсти. В эти цифры входят как изолированные переломы нижней челюсти, так и переломы с одновременными повреждениями других костей лицевого скелета.
Специалисты прогнозируют, что число повреждений нижней челюсти будет только расти, равно как и усложнится характер таких травм. Этому способствует рост числа транспортных средств, увеличение их скоростного режима, а также сложная техническая оснащенность на производствах.
Виды и локализация переломов нижней челюсти
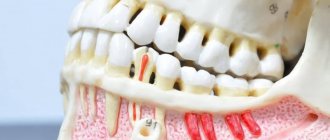
Неогнестрельные, чаще линейные переломы нижней челюсти происходят в области мыщелкового отростка, угла нижней челюсти, центральных резцов, клыка и подбородочного отверстия. Эти места принято называть «местами слабости».
Прямые переломы нижней челюсти возникают в месте приложения силы.
Отраженные переломы своей локализацией обязаны направлению удара и площади поражения. Например, вследствие бокового удара нередко возникает отраженный односторонний перелом шейки нижней челюсти. Максимальное напряжение в костной ткани на участке срединной линии создается из-за двустороннего сжатия нижнечелюстной кости в области моляров (шестые, седьмые и восьмые зубы).
То, как будут располагаться отломки при переломе нижней челюсти, зависит от нескольких факторов. В их числе: сила повреждающего фактора, объем травмируемого участка, а также группы мышц, прикрепленных к поверхности участка травмы.
Показания к проведению закрытого очагового остеосинтеза
Закрытый очаговый остеосинтез может использоваться в качестве лечения челюсти, если отломки при переломе без смещения легко могут быть вправлены руками.
Показаниями к использованию спиц Киршнера во время остеосинтеза являются все легкие переломы челюсти с возможностью фиксации отломков при помощи спиц. При этом длина спицы в отломке должна составлять не меньше 3 сантиметров.
При существенном наклоне щели перелома в переднезаднем направлении показано проведение закрытого остеосинтеза с выполнением окружающего шва. Шов исполняется таким образом, чтобы отломки были плотно сжаты в вертикальном направлении и не смещались друг относительно друга впоследствии. Иногда данный метод остеосинтеза дополняется наложением зубонаддесневого протеза.
Причины переломов нижней челюсти
Травмы нижней челюсти делятся на четыре типа:
1. Бытовые травмы, которые возникают при конфликтах в быту, выполнении работы по дому.
2. Уличные травмы, полученные при использовании транспортных средств, и уличные травмы, не связанные с повреждениями на транспорте. Это могут быть падения при ходьбе по причине гололеда, иной непогоды, или плохого самочувствия.
3. Спортивные травмы, полученные при занятиях спортом.
4. Производственные травмы, полученные на промышленном производстве в сельском хозяйстве.
Симптомы перелома нижней челюсти
При переломе нижней челюсти пациенты могут жаловаться на нарушение или ограничение подвижности нижней челюсти, боли, которые могут усиливаться при движении, откусывании или жевании, нарушение прикуса, изменение чувствительности кожи на нижней губе или подбородке, кровотечение из полости рта – характерный для разрывов слизистой оболочки симптом.
Спектр жалоб, которые предъявляет пациент, помогает врачу понять, о каком повреждении идет речь, и предположить локализацию перелома.
Диагностика переломов нижней челюсти
Диагностика основана на данных осмотра и сборе жалоб пациента.
При осмотре врач обращает внимание на состояние кожных покровов, отмечает, если ли у пациента ушибы, ссадины или раны, фиксирует наличие гиперемии, синюшности и кровоподтеков. Отмечает наличие на поврежденной стороне лица асимметрии.
При подозрении на перелом нижней челюсти врач ощупывает кончиками пальцев сначала неповрежденный участок, а затем поврежденный. Он отмечает места наибольшей болезненности, неровности, нарушение целостности, определяет амплитуду движения головки нижней челюсти в суставной впадине – для этого врач помещает кончик пальца в наружный слуховой проход. Состояние головки нижней челюсти или ее смещение врач определяет, прощупывая поверхность впереди козелка уха как в движении, так и в покое.
Нарушение целостности нижней челюсти подтверждает ряд симптомов, связанных с болью в области перелома:
Симптом отраженной боли
(непрямой нагрузки), при котором боль в области перелома возникает в ответ на давление пальцами на подбородок.
Симптом шпателя
провоцирует боль в месте перелома челюсти, причем как нижней, так и верхней. Для этого деревянный шпатель помещают между зубами пациента, после чего зубы смыкают, и врач делает небольшой удар по наружной части шпателя.
Возникновение боли при одновременном надавливании и сближении углов нижней челюсти может говорить о переломе подбородочного отдела.
Нарушение болевой и тактильной чувствительности кожи нижней губы и подбородка может говорить о повреждении нижнего альвеолярного нерва.
Для переломов нижней челюсти характерно изменение прикуса (смыкание зубов верхней и нижней челюстей происходит неправильно), которое зависит от характера и места перелома.
Так, при одностороннем переломе в области тела или угла нижней челюсти смыкание зубов будет происходить на малом отломке.
Для одностороннего перелома со смещением мыщелковых отростков характерно смыкание коренных зубов только на поврежденной стороне, а на неповрежденной – контакт не происходит.
При двустороннем переломе углов или тела нижней челюсти контакт возможен между молярами, при этом передние зубы сомкнуться не могут – у пациента отмечается открытый прикус.
Для перелома в центральном отделе нижней челюсти нарушение прикуса может не возникнуть. Но если имеется смещение отломков, у пациента появится наклон жевательных зубов в сторону языка (бугорковый контакт).
На изменение прикуса также может указывать смещение средней линии между центральными резцами на верхней и нижней челюстях, и несовпадение положения уздечки верхней и нижней губы.
Осмотр полости рта помогает найти разрывы слизистой оболочки альвеолярного отростка, а также обнаружить кровоизлияния в область переходной складки (нередко с обнажением кости). Пальпация позволяет определить расположение под слизистой оболочкой острых краев и подтверждает аномальную подвижность нижней челюсти. Если имеются смещенные отломки, то врач визуально фиксирует в линии перелома шейку или корень зуба.
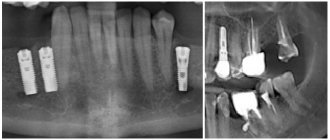
После осмотра характер и место перелома подтверждают при помощи рентгена (снимки делают в прямой и боковой проекциях) или с помощью мультиспиральной компьютерной томографии. Ортопантомография не всегда позволяет на одном снимке увидеть все изменения, возникающие при травме нижней челюсти. Следует обратить внимание, что при переломах в области угла, если смещение отломков происходит наружу, ортопантомограмма может не показать смещение. Ее следует рассматривать как две боковые рентгенограммы, к которым необходимо дополнительно провести рентгенографию в прямой проекции.
Снимки, полученные при ортопантомографии, могут быть использованы в качестве боковых проекций, но всегда требуют дополнительного снимка в прямой проекции, полученного при помощи рентгенографии.
На рентгеновском снимке лучше отображается нарушение целостности костной ткани, наличие корня зуба в щели перелома.
После проведения визуализирующего обследования врач устанавливает окончательный диагноз и определяет план лечения пациента.
Введение
Травмы челюстно-лицевой области продолжают оставаться одной из актуальных хирургических проблем, что связано с увеличением числа больных с переломами костей лицевого черепа в результате дорожно-транспортных происшествий и бытовых конфликтов, утяжелением этого вида патологии, ростом множественных и сочетанных повреждений [1, 2]. Согласно данным специализированной литературы, удельный вес челюстно-лицевой травмы в структуре различных травм среди городского населения составляет 3,2—8,0% [3]. На долю переломов нижней челюсти приходится до 85% от общего числа переломов костей лицевого черепа [4—7]. Разработка и внедрение новых способов фиксации фрагментов кости существенно повысили эффективность хирургического лечения у обсуждаемой категории пациентов, тем не менее, по данным ряда авторов, осложнения составляют от 5,2 до 38,4% случаев [8—11].
Многие из предложенных методик успешно используются в повседневной практике для проведения остеосинтеза при переломах лицевого черепа — накостные титановые пластины, шов кости проволокой из нержавеющей стали либо тантала, спицы Киршнера, возможна комбинация шва кости и спицы, фиксирующие конструкции из материалов с памятью формы. Целью данной статьи является описание клинического применения скобок с памятью формы из никелида титана (нитинол) при переломе нижней челюсти в области угла.
Клинический случай
Пациент Т.
, 41 года, поступил в клинику челюстно-лицевой хирургии Университетской клинической больницы (УКБ) № 2 Первого МГМУ им. И.М. Сеченова с жалобами на боли в области нижней челюсти справа, усиливающиеся при жевании и открывании рта, отеком лица справа, нарушением прикуса.
Из анамнеза установлено, что травма была получена в результате драки с неизвестным за 8 ч до обращения в стационар. Пациент коммоционных явлений не отмечал. Обратился в травматологический пункт, в котором произведены рентгенография черепа и межчелюстная фиксация с помощью назубных шин Тигерштедта. Бригадой скорой медицинской помощи пациент доставлен в клинику УКБ № 2 Первого МГМУ им. И.М. Сеченова, госпитализирован в экстренном порядке.
При поступлении: общее состояние относительно удовлетворительное. Соматический статус без особенностей. При осмотре определялся выраженный отек мягких тканей в околоушно-жевательной, щечной и поднижнечелюстной областях справа. Кожные покровы в складку собирались с трудом, отмечалась локальная болезненность при пальпации. Регионарные лимфатические узлы не увеличены. Симптом прямой и непрямой нагрузки положительный в области угла нижней челюсти справа. Симптом Венсана был положительным справа. Со стороны полости рта: открывание ограничено до 2 см, отмечалось нарушение смыкания зубов по типу открытого прикуса справа. Визуализировались разрывы слизистой оболочки альвеолярной части нижней челюсти в области 4.7—4.8 зубов, а также наличие геморрагических сгустков в полости рта. Глотание свободное, умеренно болезненное (рис. 1, 2,
Рис. 1. Внешний вид пациента Т. при госпитализации.
Рис. 2. Ортопантомограмма пациента Т. при госпитализации. Определяется нарушение целостности костной ткани в области угла нижней челюсти справа с наличием зуба 4.8 в линии перелома. 3).
Рис. 3. Рентгенограмма черепа пациента Т. в прямой проекции.
На основании жалоб, анамнеза, данных клинического осмотра и рентгенологического обследования поставлен диагноз: «Перелом нижней челюсти в области угла справа со смещением отломков».
После дообследования и предоперационной подготовки в день поступления в стационар пациенту выполнено оперативное вмешательство: остеосинтез нижней челюсти в области угла справа наружным доступом с помощью скобок из никелида титана.
Операцию проводили следующим образом: на фоне премедикации в условиях местной анестезии с Sol. Lidocaini 1% 20 мл, на стороне перелома параллельно краю нижней челюсти, отступив на 2 см в области угла, выполнен разрез кожи длиной 4 см. Послойно рассечены кожа, подкожно-жировая клетчатка, поверхностная фасция шеи и m. рlatisma. У места прикрепления к углу нижней челюсти была отсечена собственно жевательная мышца. Скелетирована нижняя челюсть в области угла. После визуализации линии перелома проведено удаление мелких костных фрагментов, устранена интерпозиция мягких тканей, удалены сгустки крови. Перед проведением остеосинтеза нижней челюсти удален свободнолежащий фрагмент кости и зуб 4.8 из линии перелома (рис. 4),
Рис. 4. Удаленный фрагмент кости, не связанный с надкостницей, и зуб 4.8 из линии перелома. выполнена репозиция фрагментов кости. Проведены фиксация прикуса в привычном для больного положении при помощи резиновых тяг и остеосинтез с помощью двух скобок из никелида титана Ω- и S-образной формы под контролем прикуса (рис. 5).
Рис. 5. Этап операции. Остеосинтез нижней челюсти с помощью скобок из никелида титана Ω- и S-образной формы.
Скобки устанавливали следующим образом: бикортикально формировали отверстия на каждом фрагменте с помощью сверла, далее предварительно охлажденные до +1—3 °С ножки скобки разгибали в стороны (активировали скобку) и вводили в соответствующие фрезевые отверстия. При нагревании скобки до 35—36 °С происходило восстановление первоначальной формы — сближение ножек скобки, что приводило к дозированной компрессии фрагментов кости. Послеоперационную рану обрабатывали растворами антисептиков, устанавливали латексный выпускник. Рану послойно ушивали. По ходу операции осуществляли гемостаз.
Послеоперационный период протекал без особенностей. Пациент был выписан на амбулаторное наблюдение на 7-е сутки после операции, после снятия швов. Открывание рта на момент выписки составляло 3,0 см.
На 2-е сутки после операции выполнены контрольные рентгенограммы черепа в прямой проекции и ортопантомография. Положение костных фрагментов и фиксирующих конструкций было правильным, вторичных смещений не выявлено (рис. 6,
Рис. 6. Ортопантомограмма пациента Т. после хирургического лечения. 7).
Рис. 7. Рентгенограмма черепа пациента Т. в прямой проекции после хирургического лечения.
При контрольном осмотре через 1 мес отмечено увеличение открывания рта до 4,2 см, жевательная функция и внешний вид пациента были восстановлены полностью (рис. 8).
Рис. 8. а — внешний вид пациента Т. через 1 мес после операции; б — амплитуда открывания рта пациента Т. через 1 мес после операции. В результате динамического наблюдения и междисциплинарного лечения совместно с физиотерапевтом, назначения физио- и витаминотерапии на пораженной стороне чувствительность кожных покровов и зубов в зоне иннервации нижнеальвеолярного нерва была восстановлена через 6 мес.
За трехлетний период наблюдения с проведением осмотров 1 раз в 6 мес отмечены стабильное состояние прикуса, отсутствие болей в области нижней челюсти и нейропатии нижнеальвеолярного нерва.
Первая помощь при переломах нижней челюсти
Может проводится как на месте происшествия, так и в машине скорой помощи. Ее могут оказывать как медицинские работники, так и не медицинские в порядке взаимопомощи.
Пострадавшему временно (на несколько часов) фиксируют поврежденную челюсть (прижимают верхнюю к нижней) при помощи повязок или иных приспособлений, чтобы получить возможность доставить его в лечебное учреждение.
Для фиксации могут быть использованы: круговая бинтовая теменно-подбородочная повязка, мягкая подбородочная праща (Померанцевой – Урбанской), шина Энтина (стандартная транспортная жесткая повязка), а также разные виды межчелюстного лигатурного связывания. При наличии у пациента черепно-мозговой травмы лигатурное связывание используют с крайней осторожностью — зафиксированные челюсти не позволяют открыть рот, и могут привести к аспирации рвотными массами или кровью.
Техника внутрикостного (погружного остеосинтеза)
Проводится открытая и закрытая операция в зависимости от тяжести перелома. При закрытой операции сначала сопоставляются отломки костной ткани при помощи аппарата. На следующем этапе плавно вставляется металлический стержень в тело трубчатой кости. Для этого специалисты используют рентген, чтобы достичь 100% точности. Завершающим этапом является извлечение проводника и наложение хирургических швов.
Открытая операция проводится после вскрытия тканей. Отломки ровно фиксируются хирургическим инструментом (специальные аппараты не используются). Данный метод эффективнее, но травматичнее. Повреждение мягких тканей, обширная кровопотеря и вероятность инфицирования заставляют пациентов отказаться от данного метода.
Постоянная фиксация отломков
Зафиксировать отломки нижней челюсти можно с помощью консервативных и хирургических методов.
Постоянная фиксация может быть проведена при помощи: стальных стандартных ленточных шин (шины Васильева), назубных проволочных шин Тигерштедта, назубных зубодесневых и наддесневых шин из пластмассы, которые изготавливают в зуботехнических лабораториях (в настоящее время они используются редко).
В последние годы в некоторых клиниках стали применяться ортодонтические винты, которые вводятся через слизистую в альвеолярные отростки челюстей по 3 штуки с каждой стороны, после чего на головки винтов надевают резиновую тягу, обеспечивающую межчелюстную фиксацию. Это позволяет избежать трудоемкой процедуры двухчелюстного шинирования. С другой стороны, при введении винтов можно повредить корни зубов, кроме того, нередки ситуации, когда винт под действием резиновой тяги, становится подвижным, что приводит к неполноценной межчелюстной фиксации и удалению винта.
Если консервативные способы лечения не дали эффекта, применяется остеосинтез – это хирургический метод, который при помощи приспособлений позволяет зафиксировать отломки и устранить их подвижность. Остеосинтез проводят, если у пациента имеются оскольчатые переломы нижней челюсти, или смещение отломков настолько выражено, что они не дают возможности провести закрытую репозицию. Также остеосинтез показан при отсутствии или недостаточном количестве зубов у пациента.
Примерно 30% пациентов с переломами нижней челюсти требуется хирургическое лечение. В настоящее время остеосинтез является одним из ведущих способов хирургической помощи, и применяется намного чаще, чем в прошлом.
Это связано как с увеличением арсенала технических средств для проведения операции (наличие физиодиспенсеров, титановых минипластин), что ведет к улучшению техники проведения хирургических вмешательств, большей предсказуемости результатов, так и с запросами пациентов, которые направлены на более комфортное течение посттравматического периода, уменьшение времени межчелюстной фиксации, а в некоторых случаях на полный отказ от нее.
Методы лечения переломов при помощи хирургических методик позволяют сопоставить и зафиксировать подвижные костные фрагменты в нормальное анатомическое положение. Это помогает сократить сроки лечения и добиться раннего восстановления функции нижней челюсти. Однако, по разным данным российских и зарубежных клиник, имеет место и отрицательный момент применения остеосинтеза – порядка 30% пациентов сталкивается с осложнениями после использования данной методики. Это связано с использованием материалов для удерживания отломков: сталь, титан и т.д. Даже самые биоинертные сплавы не являются идеальными. Находясь в костной ткани, они подвергаются коррозии и вызывают явления гальваноза, что отрицательно влияет на процессы восстановления может вызвать гнойно-воспалительные осложнения и болевые реакции.
Компрессионно-дистракционный остеосинтез костей лицевого скелета у детей
В настоящее время возросла обращаемость детей с врожденными и приобретенными дефектами и деформациями челюстно-лицевой области. При этом нарушаются такие жизненно важные функции, как дыхание, зрение, жевание, глотание, речь. При выраженном недоразвитии нижней челюсти у детей корень языка смещается кзади и сужает просвет верхних дыхательных путей, результатом чего является нарушение дыхания, чаще во время сна, что может привести к летальному исходу ребенка. Дети с косметическими недостатками становятся стеснительными, подавленными, скрытными, необщительными. Кроме того, серьезные душевные страдания приводят к их агрессивности и озлобленности. Не устраненные в детском возрасте недоразвития и дефекты отдельных костей лица вызывают грубые вторичные деформации, которые не всегда и с большим трудом поддаются коррекции в более старшем возрасте.
Сегодня отсутствует единый хирургический метод лечения, позволяющий надежно устранять различные деформации лица, связанные с недоразвитием и дефектами костей черепа. Выполняемые костно-пластические операции с использованием трансплантатов различного типа, титановых пластин, биокомпозитов, силикона недостаточно надёжны при устранении деформаций, дефектов и недоразвитии костей лицевого скелета и часто неприемлемы для детей различного возраста. При одномоментном перемещении костей средней зоны лица, помимо рецидивов, возникают более тяжелые осложнения: значительные проффузные кровотечения, частичные омертвения костных фрагментов и даже летальные исходы.
В последнее десятилетие в мире интенсивное развитие получает метод компрессионно-дистракционного остеосинтеза (КДО) в челюстно-лицевой области, так как этот способ не приводит к развитию осложнений, возникающих при выполнении костной пластики (Ha bal M.B., 1995; McCor mick S.U., 1995; Cohen S.R., 1995; Pol ley J., 1995; Mo na ste rio O., Mo li na F., 1997; Klein C.,1998; Boz zet ti
A. et al., 2001; Mi no ru U., 2001; Mo li na F., 2004; Ha ra da K., 2007).
На сегодняшний день разработано достаточно много методов лечения и компрессионно-дистракционных аппаратов (КДА) для детей с недоразвитием и дефектами нижней челюсти (Рогинский В.В. и со авт., 2001, 2002, 2007).
В 1954 г. Г.А. Илизаровым был предложен метод для лечения пациентов с различными врождёнными и приобретенными деформациями трубчатых костей.
Проведение КДО возможно только с применением КДА. Громоздкость отечественных дистракционных аппаратов и сложность их изготовления привели к тому, что в нашей стране КДО не получил должного развития, в результате в течение многих лет тысячи пациентов не получили качественного полноценного лечения. Отставание от стран Запада, несмотря на отечественный приоритет КДО, составило 20-30 лет. Нуждаемость в этом виде помощи только среди детей Москвы составляет около 500 человек в год, а в целом по России — это несколько сотен тысяч человек.
Несмотря на то, что во всем мире для лечения взрослых пациентов успешно используется КДО, остается много важных нерешенных вопросов, касающихся лечения детей: режим дистракции в зависимости от зоны патологии; возраст, в котором возможно применение данного метода; необходимость разработки наиболее
щадящих методик оперативных вмешательств к отдельным зонам лицевого скелета; отсутствие четких показаний и противопоказаний к применению метода и использованию различных видов КДА. Кроме того, до сих пор не ясно, как влияет КДО на морфогенез тканей челюстно-лицевой области у детей в процессе их роста, не разработаны наиболее надежные и удобные в применении КДА, позволяющие уменьшить процент осложнений.
Показания к использованию медицинской технологии
Использование КДО на нижней челюсти:
1. Недоразвитие ветви и/или тела нижней челюсти, сопровождающиеся дизокклюзией.
2. Дефект тела или ветви нижней челюсти.
3. Синдром дыхательной обструкции, как следствие выраженного недоразвития нижней челюсти.
4. Сочетанное недоразвитие нижней и верхней челюстей.
5. Недоразвитие подбородочного отдела нижней челюсти.
Использование КДО на верхней челюсти:
1. Верхняя ретромикрогнатия.
2. Деформация лица во фронтальной области верхней челюсти.
Использование КДО на средней зоны лица:
1. Экзофтальм, как следствие недоразвития скулоорбитального комплекса.
Противопоказания к использованию медицинской технологии
1. Аллергические реакции на металл.
2. Остеопороз.
3. Выраженные нарушения психики.
Материально-техническое обеспечение медицинской технологии
1. Набор узлов и деталей титановых для сборки внутриротовых компрессионно-дистракционных устройств для исправления врождённых и приобретенных дефектов и деформаций верхней и нижней челюстей и инструментов для установки НУД-КД/ВНЧ — «Конмет» (, Россия). Регистрационное удостоверение ФС № 022а4337/098704 от 20.12.2004 г.
2. Набор узлов и деталей титановых для сборки устройств наружной фиксации и дистракции при переломах и деформациях нижней челюсти, инструментов и приспособлений для их установки, НУД-ФД/НЧ — «Конмет» (, Россия). Регистрационное удостоверение ФС № 022а4339/0988-04 от 20.12.2004 г.
3. Набор узлов и деталей титановых для сборки устройств дистракционных наружной фиксации при переломах костей средней зоны лица и верхней челюсти и инструментов для их установки, НЭ-Д/СЗВЧ — «Конмет» (, Россия). Регистрационное удостоверение ФС № 022а4338/0989-04 от 20.12.2004 г.
Описание медицинской технологии
Способ устранения недоразвития и/или дефекта нижней челюсти, сочетающегося с недоразвитием верхней челюсти (Патент РФ на изо бре те ние № 2267303).
Подготовка пациентов к плановой операции проводится по общим правилам: общий анализ крови с гемосиндромом, группа крови и резус-фактор, биохимический анализ крови, общий анализ мочи, электрокардиограмма. Основными этапами предоперационного обследования являются рентгенологическое (телерентгенограммы в двух проекциях, ортопантомограмма, компьютерная томография), цефалометрия, фотодокументация.
Операция проводится под эндотрахеальным наркозом. Разрезом до 6 см в полости рта по переходной складке на стороне поражения скелетируют ветвь нижней челюсти. Намечют линию остеотомии: бором или пилой распиливают наружный кортикальный слой, а по переднему и заднему краю ветви нижней челюсти распиливают наружную и внутреннюю кортикальные пластинки (внутренняя кортикальная пластинка в средней части сохраняется). Устанавливают внутриротовой накостный КДА, предварительно раскрученный на 2 — 3 мм, для того чтобы в последующем можно было провести компрессию. Сверлом диаметром 1,6 мм формируют отверстия под винты. Отверстия сверлят через 2 кортикальных слоя. Глубиномером определяют протяженность отверстий. На основании этого подбирают самонарезающие винты необходимой длины диаметром 2 мм. Аппарат фиксируют к костным фрагментам так, что винты проходят через 2 кортикальных слоя. Винты закручивают до упора. Остеотомом надламывают внутреннюю кортикальную пластинку. Осуществляют компрессию костных фрагментов. Гемостаз проводится по ходу операции. Рану послойно ушивают.
Затем делают разрез по переходной складке от бугра верхней челюсти одной стороны до бугра противоположной стороны. Скелетируют верхнюю челюсть с двух сторон. К верхней челюсти на пораженной стороне фиксируют внутриротовой на костный КДА не менее 12 шурупами диаметром 2 мм и длиной не более 5-7 мм. Аппарат фиксируется под углом к средней линии так, чтобы во время дистракции обеспечить расхождение костных отломков в виде клина, вершина которого расположена в области скулоальвеолярного гребня здоровой стороны. Выполняют остеотомию сошника, а так же верхней челюсти на уровне грушевидных отверстий с двух сторон с проведением остеотомии в области крыловерхнечелюстного сочленения на здоровой и пораженной стороне (рис. 1). Проводится компрессия. Осуществляется гемостаз походу операции. Рану послойно ушивают.
Рис. 1. Схемы разработанной методики: а — операция; б — полученный результат.
В послеоперационном периоде проводится антибактериальная терапия, полоскание рта раствором антисептика, ежедневная смена асептических повязок. Дистракцию нижней челюсти начинают на 5-е сутки после операции по 1 мм в день за 4 приёма по 0,25 мм; дистракцию верхней челюсти — на 10-е сутки по 0,5 мм в день за 2 приёма по 0,25 мм. Период ретенции длится не менее 12 недель.
Способ устранения недоразвития подбородочного отдела нижней челюсти (Патент РФ на изобретение № 2268016).
Подготовка пациентов к плановой операции осуществляется по общим правилам: общий анализ крови с гемосиндромом, группа крови и резусфактор, биохимический анализ крови, общий анализ мочи, электрокардиограмма. Главными этапами предоперационного обследования являются рентгенологическое (телерентгенограммы в двух проекциях, ортопантомограмма, компьютерная томография), цефалометрия, фотодокументация.
Операция проводится под эндотрахеальным наркозом. Разрезом в полости рта по переходной складке от ретромолярной области одной стороны до ретромолярной области другой стороны скелетируют тело нижней челюсти с двух сторон. Осторожно мобилизовывается сосудисто-нервный пучок с двух сторон. В области угла нижней челюсти устанавливают КДА параллельно нижнему краю тела, предварительно раскрученный на 1-2 мм, для того чтобы в последующем можно было провести компрессию. Сверлом диаметром 1,6 мм формируют отверстия под винты. Отверстия сверлят через 2 кортикальных слоя. Глубиномером определяют протяженность отверстий. Учитывая это, подбирают самонарезающие винты необходимой длины диаметром 2 мм. Аппарат фиксируют к костным фрагментам 6 винтами так, что последние проходят через 2 кортикальных слоя. Винты закручивают до упора. Винт аппарата выводится наружу через отдельный разрез
(0,3 мм) на коже в заушной области. Аналогичным способом фиксируют второй КДА в области угла нижней челюсти с другой стороны. С помощью осциллирующей пилы выполняют продлённую остеотомию подбородочного отдела: после подбородочного отдела линия остеотомии идёт через тело до угла нижней челюсти с двух сторон. Линия остеотомии проходит ниже корней и зачатков зубов. Проводят компрессию костных фрагментов (рис. 2). Гемостаз осуществляется по ходу операции. Рану ушивают. Накладывают шов на рану в области выхода винта аппарата на коже.
Рис. 2. Схемы разработанного способа: а — операция; б — полученный результат.
В послеоперационном периоде проводится антибактериальная терапия, полоскание рта раствором антисептика, ежедневная смена асептических повязок.
Дистракцию начинают на 5-е сутки после операции по 0,5 мм в день за 2 приёма по 0,25 мм. Период ретенции длится не менее 12 недель.
Способ одновременного устранения недоразвития ветви и тела нижней челюсти
Осуществляется подготовка пациентов к плановой операции по общим правилам: общий анализ крови с гемосиндромом, группа крови и резус-фактор, биохимический анализ крови, общий анализ мочи, электрокардиограмма. Основные этапы предоперационного обследования: рентгенологическое (телерентгенограммы в двух проекциях, ортопантомограмма, компьютерная томография), цефалометрия, фотодокументация.
Проводится операция под эндотрахеальным наркозом. Разрезом до 6 см в поднижнечелюстной области на стороне поражения скелетируют нижнюю челюсть. Намечают линию остеотомии в области ветви и тела: бором или пилой распиливают наружный кортикальный слой, а по переднему и заднему краю ветви нижней
челюсти распиливают наружную и внутреннюю кортикальные пластинки (внутренняя кортикальная пластинка в средней части сохраняется). Устанавливают накостные КДА, предварительно раскрученные на 2 — 3 мм, для того чтобы в последующем можно было провести компрессию. Аппарат в области ветви нижней челюсти
устанавливают параллельно её заднему краю, а на теле — параллельно окклюзионной плоскости; кроме того, винт аппарата выводят наружу через отдельный разрез (0,3 мм) на коже в заушной области. Сверлом диаметром 1,6 мм формируют отверстия под винты. Отверстия сверлят через 2 кортикальных слоя. Глубиномером определяют протяженность отверстий. С учетом этого подбирают самонарезающие винты необходимой длины диаметром 2 мм. Аппараты фиксируют к костным фрагментам так, что винты
проходят через 2 кортикальных слоя. Винты закручивают до упора. Остеотомом надламывают внутреннюю кортикальную пластинку. Выполняют компрессию костных фрагментов. Гемостаз осуществляют по ходу операции. Рану послойно ушивают (рис. 3).
Рис. 3. Схема разработанного способа: а — операция; б — полученный результат.
Проводится антибактериальная терапия, ежедневная смена асептических повязок в послеоперационном периоде.
Дистракцию начинают на 5-е сутки после операции по 1 мм в день за 4 приёма по 0,25 мм. Период ретенции — не менее 12 недель.
Устранение недоразвития средней зоны лица
Подготовка пациентов к плановой операции проводится по общим правилам: общий анализ крови с гемосиндромом, группа крови и резус-фактор, биохимический анализ крови, общий анализ
мочи, электрокардиограмма. Основными этапами предоперационного обследования являются рентгенологическое (телерентгенограммы в двух проекциях, ортопантомограмма, компьютерная то-
мография), цефалометрия, фотодокументация.
Операцию выполняют под эндотрахеальным наркозом. Перед операцией мальчиков бреют налысо, а девочкам выбривают волосы в виде дорожки шириной около 4 см вдоль предполагаемого разреза. Применяется двусторонний трансвенечный доступ. Линия разреза — волнистая. Перед разрезом проводится гидропрепарирование тканей. Скелетируют лобную кость таким образом, чтобы надкостница оставалась за 2 см до верхнего края орбит. Выделяют от мышц височную и подвисочную ямки с двух сторон. Скелетируют корень носа и носовые кости. Очень осторожно выделяют крышу и дно орбит. При скелетировании медиальных стенок орбит тщательно выделяют носослёзный канал, а также накладывают лигатуру в области кантальных связок, чтобы при ушивании раны фиксировать их в нужном месте. С
помощью осциллирующей пилы выполняют остеотомию по линии лобно-носового шва, продолжая линию остеотомии вниз через костную часть носослёзного канала (не повреждая мягкотканную часть
канала), дно орбиты. Далее распил проводят вверх, вдоль латерального края глазницы и заканчивают на уровне лобноскулового шва. Также с помощью осциллирующей пилы проводят остеотомию скуловой дуги ближе к скуловой кости в наиболее широкой её части. Затем с помощью 3 небольших разрезов в полости рта по переходной складке верхней челюсти осуществляют доступ к сошнику и крыловерхнечелюстным сочленениям. Проводят остеотомию сошника и в области крыловерхнечелюстного сочленения с двух сторон. С помощью изогнутого долота выполняют остеотомию в области корня носа по вертикальной пластинке решётчатой кости и сошнику. В этот момент необходимо быть предельно осторожными и не повредить эндотрахеальную трубку. После того как выполняют все распилы, при помощи щипцов Rowe проводят мобилизацию комплекса средней зоны лица.
Накостный аппарат фиксируют с помощью самонарезающих винтов к скуловой и теменной кости. При фиксации к скуловой кости используют винты диаметром 2 мм и длиной 7 мм, а при фиксации к теменной кости — винты диаметром 2 мм и длиной 5 мм. После фиксации аппаратов проводят компрессию. Важно отметить, что аппараты устанавливаются параллельно скуловым дугам. Тщательный гемостаз осуществляют по ходу всей операции. Рану послойно ушивают.
В послеоперационном периоде проводят антибактериальную терапию, тщательный туалет полости рта и ежедневную смену асептических повязок.
Дистракцию начинают на 7-е сутки после операции по 1 мм в день за 4 приёма по 0,25 мм. После то го, как достигается необходимый функциональный и косметический результат, дистракцию прекращают. Длительность периода ретенции составляет в среднем 12 не дель.
Возможные осложнения при использовании медицинской технологии и способы их устранения
1. Отсутствие костного регенерата. Индивидуальный ритм и темп дистракции, повторная дистракция.
2. Остеомиелит или воспаление мягких тканей в области аппарата, гайморит. Соблюдение правил асептики и антисептики, антибактериальная терапия, досрочное удаление аппарата.
3. Поломка аппарата. Замена аппарата. Повторная дистракция.
4. Неправильный вектор дистракции и как следствие нарушение эстетики лица или несоответствие функционального результата должному. Повторная корригирующая операция.
Эффективность использования медицинской технологии
Метод КДО применён у 198 больных с недоразвитием и/или дефектами различных костей черепа врожденного и приобретенного характера в возрасте от 14 дней до 17 лет. Из них с недоразвитием и/или дефектами нижней челюсти врожденного или приобретенного характера было 156 детей; с недоразвитием верхней челюсти после хейлоуранопластики по поводу врождённой односторонней расщелины верхней губы, альвеолярного отростка и нёба — 16; с недоразвитием верхней челюсти после хейлоуранопластики по поводу врождённой двусторонней расщелины верхней губы, альвеолярного отростка и нёба — 12 детей; с синдромом Биндера — 2; с синдромом Крузона — 10; с синдромом Апера — 1 ребёнок; с плагиоцефалией — 1 пациент. Операции выполняли по жизненным, функциональным и косметическим показаниям.
В результате применения метода КДО получены следующие результаты: хороший — у 77,3%, удовлетворительный — у 13,6% больных и отрицательный — у 9,1% детей (рис. 4). При хороших и
удовлетворительных результатах длина костного регенерата составляла 10 — 40 мм.
Рис. 4. Диаграмма полученных результатов.
Во время удлинения ветви нижней челюсти без дистракции верхней челюсти формируется открытый прикус на стороне поражения от 7 до 12 мм.
После удаления КДА уже через 1 мес открытый прикус не определяется, что связано не с ростом верхней челюсти, как считали раньше, а с сокращением регенерата за счёт действия жевательных мышц. Размер сокращения составляет 40-50% от первоначальной длины. Таким образом, чтобы избежать данного вида
осложнения, необходимо одновременно удлинять ветвь нижней челюсти с верхней челюстью. Необходимость в дистракции верхней челюсти при врожденной патологии составляет 75%, а при приобретенной — 30%.
Предложенный способ по одновременному устранению недоразвития нижней и верхней челюстей имеет следующие преимущества:
— значительно снижен возрастной ценз, способ можно применять с 1,5 лет;
— отсутствует межчелюстная фиксация;
— сохранена функция верхней и нижней челюстей, что оказывает положительное влияние на формирование регенерата;
— возможность полноценного питания и адекватный уход за полостью рта;
— приемлемый внешний вид пациента;
— отсутствуют послеоперационные рубцы на коже;
— неограничен период ретенции;
— значительно снижается риск развития воспалительных процессов;
— возможность проведения независимой друг от друга дистракции верхней и нижней челюстей с индивидуальным графиком дистракции для каждой из челюстей.
У детей с двусторонним недоразвитием и/или дефектом нижней челюсти врождённого или приобретенного характера всегда определяется недоразвитие подбородочного отдела, особенно это касается больных с синдромом Тричера-Коллинза и пациентов, длительно страдающих двусторонним анкилозирующим поражением височно-нижнечелюстного сустава. После устранения двустороннего недоразвития или дефекта нижней челюсти и восстановления конструктивного прикуса около 70% детей нуждаются в хирургической коррекции подбородочного отдела.
Известны многочисленные способы гениопластики с использованием аутотрансплантатов, аллотрансплантатов, пластики с применением эндопротезов из различных синтетических материалов (ЭГМАСС-12, силикон, ПолиГап).
Способ устранения недоразвития подбородочного отдела нижней челюсти имеет следующие преимущества:
— существенно уменьшился возрастной ценз, способ можно применять с 5-6 лет;
— отсутствие возможных отрицательных моментов, характерных для методов с использованием различных видов трансплантатов;
— отсутствие инородного материала;
— гениопластика выполняется исключительно местными тканями;
— прогнозируемый результат, возможность изменения положения подбородочного фрагмента нижней челюсти в зависимости от пожеланий пациента и родителей в процессе дистракции.
Дети с врождённой и приобретенной патологией нижней челюсти в 80% случаях нуждаются в устранении недоразвития и/или дефекта не только ветви, но и тела нижней челюсти. Существующие двухэтапные методы значительно увеличивают сроки лечения.
Преимущества способа одновременного устранения недоразвития ветви и тела нижней челюсти:
— приемлемый внешний вид пациента;
— отсутствуют дополнительные послеоперационные рубцы на коже от стержней;
— неограничен период ретенции;
— существенно снижается риск развития воспалительных процессов;
— облег чен уход за КДА.
Накостный КДА для средней зоны лица имеет преимущества:
— обеспечение жёсткой фиксации костных фрагментов во время периодов дистракции и ретенции, что является одним из основных условий созревания костного регенерата;
— возможность осуществить компрессию костных фрагментов после их остеотомии, что является основной профилактикой послеоперационных кровотечений;
— строго дозированное перемещение, т.е. размер регенерата всегда соответствовал срокам дистракции, например, при дистракции в течение 20 дней по 1 мм в сутки длина регенерата была 20 мм;
— вес аппарата 5 г;
— приемлемый внешний вид пациента;
— обычная гигиена полости рта;
— простой уход за дистракционным аппаратом во время дистракции и ретенции;
— не ограничен период ретенции;
— возможность применения КДА в раннем детском возрасте;
— возможно изменение положения средней зоны лица в зависимости от пожеланий пациента и родителей в процессе дистракции.
Таким образом, применение КДО в настоящее время позволяет существенно повысить эффективность лечения детей со сложной челюстно-лицевой патологией врожденного и приобретенного характера, а также даёт возможность оказать реальную лечебную помощь детям с деформациями и дефектами лицевого черепа с использованием щадящего метода.
Метод КДО является приоритетным в детской практике и дальнейшая его разработка и внедрение позволяет считать его основным при лечении детей с дефектами и деформациями челюстно-лицевой и краниофациальной областей.
Широкое внедрение метода дистракции позволит значительно повысить эффективность и результативность реконструктивных оперативных вмешательств, сократить сроки реабилитации и пребывания пациентов на больничной койке. В значительной степени отпадёт необходимость в использовании эндопротезов и высокотравматичных методов устранения дефектов. Не возникает необходимости решать сложные задачи по устранению вторичных деформаций у взрослых пациентов, так как дети будут входить во «взрослую» жизнь, прошедшие комплексную реабилитацию.
Авторы:
проф. В.В. Рогинский
докт.мед.наук Д.Ю. Комелягин
канд.мед.наук С.А. Дубин
Методы остеосинтеза
Различают прямой и непрямой метод остеосинтеза.
Прямые методы:
— внутрикостный остеосинтез с использованием спиц, стержней, штифтов и винтов,
— накостный остеосинтез с применением накостных пластин, скоб, круговых лигатур, рамок,
— внутрикостно-накостный остеосинтез на основе костных швов или их сочетания со спицами и скобами.
Непрямой остеосинтез основан на использовании различных фиксирующих устройств, как накостных (костные зажимы и клеммы), так и внутрикостных (стержни, штифты, винты и спицы).
Остеосинтез могут проводить как под местной анестезией в сочетании с нейролептанальгезией и атараланальгезией, так и под общим наркозом.
Характер доступа (внеротовой или внутриротовой) определяет врач.
Если остеосинтез проводится с использованием внеротового доступа, то в случае перелома в области угла и тела нижней челюсти врач производит разрез в поднижнечелюстной области. Если перелом произошел в области фронтального отдела – разрез будет в подподбородочной области. При переломах в области мыщелкового отростка – в позадинижнечелюстной области. В ходе операции врач обнажает костные отломки, удаляет мелкие осколки, и фиксирует крупные осколки и отломки в нормальном анатомическом положении при помощи выбранной конструкции.
Если врач использует для проведения остеосинтеза внутриротовой доступ, то он осуществляет разрез слизистой вместе с надкостницей, затем проводит сопоставление отломков и выполняет остеосинтез.
Открытый очаговый остеосинтез
Костный шов
Показания для наложения: свежие переломы верхней челюсти и нижней челюсти, скуловой кости и дуги, переломы с легковправимыми отломками. Противопоказания: наличие развившегося воспалительного процесса в очаге перелома (воспалительный инфильтрат, абсцесс, флегмона), травматический остеомиелит, огнестрельные повреждения челюстей, мелкооскольчатые и косые переломы челюстей, переломы с дефектом кости. Материал: для костного шва используют проволоку из нержавеющей стали марок 1Х18Н9Т, ЭП-400, ЭЯТ-1, титана, тантала или капроновую нить диаметром 0,6-0,8 мм. Для наложения костного шва рассекают кожу и обнажают концы отломков с вестибулярной и язычной поверхности, сопоставляют их и скрепляют проволочной лигатурой, проводимой через просверленные отверстия в кости.
Иммобилизация отломков нижней челюсти: а — рентгенограмма нижней челюсти справа, боковая проекция (отломки фиксированы костным швом); б — варианты иммобилизации отломков нижней челюсти с помощью костного шва (схема)
Костные швы снимают, если в области перелома развиваются воспалительные явления (травматический остеомиелит) или образуется лигатурный свищ. Преимуществами костного шва является то, что сохраняется функция жевания, возможно соблюдение обычной гигиены полости рта, не возникают патологические состояния в области мыщелкового отростка.
Накостные металлические мини-пластины
Показания для наложения: любые переломы челюстей, за исключением мелкооскольчатых. Преимущество мини-пластинок перед костным швом состоит в том, что в ходе операции надкостница отслаивается только с одной (вестибулярной) поверхности челюсти, что значительно уменьшает нарушение микроциркуляции в области перелома. Для иммобилизации отломков челюстей используют мини-пластины различной формы и размеров. Они изготавливаются из титана или нержавеющей стали. Длина мини-пластин может колебаться в пределах от 2 до 24 см, толщина — от 1 до 1,4 мм. Шурупы для крепления минипластин имеют диаметр 2,0 и 2,3 мм и длину от 5 до 19 мм. Для наложения мини-пластин рассекают кожу и обнажают концы отломков на 2,0-2,5 см от щели перелома с вестибулярной поверхности, сопоставляют их и скрепляют пластинкой, которую прикручивают шурупами.
Рентгенограмма нижней челюсти справа, боковая проекция. Отломки фиксированы металлическими мини-пластинами
В настоящее время мини-пластины накладывают интраоральным подходом, при этом кожные покровы не рассекают.
Быстротвердеющие пластмассы (Е.Ш. Магарилл)
Показания: переломы в области тела нижней челюсти. Противопоказания: перелом мыщелкового отростка, оскольчатые переломы. Методика наложения: обнажают отломки нижней челюсти с наружной поверхности, сопоставляют в правильное положение. На их вестибулярной поверхности на протяжении 1,5 см в обе стороны от щели перелома высверливают жёлоб шириной 0,5 см на глубину кортикальной пластинки. По форме жёлоб напоминает обратный конус. Резиноподобную пластмассу пакуют в жёлоб. После застывания её излишки удаляют фрезой. Рану ушивают.
Клей остеопласт (Г.В. Головин, П.П. Новожилов)
Клей остеопласт представляет модифицированные резорциновые эпоксидные смолы с органическими наполнителями со сроком твердения при комнатной температуре 5-10 мин. Отломки после нанесения клея необходимо удерживать в неподвижном состоянии 10-15 мин до его затвердения, после чего рану ушивают.
Скобы из металла с заранее заданными свойствами (В.К. Поленичкин)
Скобы изготовливают из никелево-титановой проволоки (50,8 ат % и 49,2 ат %) диаметром 1,6 мм. Этот сплав становится мягким и легко деформируется при значительном охлаждении, но восстанавливает свою первоначальную форму и жёсткость при комнатной температуре. Скобы имеют разную форму и используются в зависимости от вида и локализации перелома. Их накладывают на обнажённые концы отломков нижней челюсти. В них сверлят сквозные каналы, отступя от щели перелома на 1,0-1,5 см, расстояние между отверстиями каналов должно быть больше, чем расстояние между «ножками скобы». Скобу охлаждают хлорэтилом, растягивают и её концы вставляют в просверлённые каналы предварительно репонированных отломков. После согревания скоба восстанавливает исходную форму, а её концы создают компрессию и иммобилизацию отломков.
Иммобилизация отломков нижней челюсти с помощью скоб из металла с заранее заданными свойствами
Спицы Киршнера
Показания: перелом тела нижней челюсти в боковом отделе при трудновправимых отломках и невозможности их репонировать руками, интерпозиции мягких тканей, перелом мыщелкового отростка со смещением отломков, переломы в области подбородка в сочетании с проволочной лигатурой. Для наложения спицы обнажают и репонируют отломки. Далее спицу проводят из одного отломка в другой не менее чем на 3 см в каждый. Кусачками спицу укорачивают, оставляя выступающие из кости концы длиной 4-5 мм. После консолидации спицу удаляют.
Комбинация костного шва и спицы
Используют для более прочной и надёжной фиксации отломков нижней челюсти.
Остеосинтез отломков верхней челюсти с помощью костного шва (а, б) и спицы (в)
Костный или проволочный шов
В 1825 году хирург Роджерс из Дублина провел первую в мире операцию с использованием серебряной проволоки. С ее помощью он соединил отломки нижней челюсти. Позднее, в 1863 году, русский хирург Ю.К. Шимановский с успехом применил костный шов. С этого момента на протяжении многих лет костный шов успешно использовался для остеосинтеза. В качестве основного материала изначально выступала нержавеющая сталь, позже ее заменили на титан, нихром, тантал и др.
Существуют различные модификации костного шва (петлеобразный, крестообразный, восьмеркообразный, трапециевидный, двойной и проч.). Выбор зависит от характера и места перелома.
Наложение костного шва происходит по определенным правилам. Отверстия под материал важно делать в тех зонах, где исключено повреждение нижнечелюстного канала и корней зубов, и не ближе 1,0 см от линии перелома. В идеале шов должен пересекать линию перелома в середине расстояния между краем нижней челюсти и основанием альвеолярного отростка.
Металлические спицы Киршнера
Впервые данный вид спиц использовали для лечения переломов нижней челюсти в 1933 году. Внутрикостное введение данных спиц может проводится как чрезкожно (без разрезов), так и с разрезами мягких тканей.
В 1975 году В.В. Донской применил оригинальную методику, с помощью которой он вводил спицу в ветвь нижней челюсти через слизистую без разреза, далее проводил репозицию, и фиксировал ее как шину к зубам или к шине. Позднее, в 1988 году Дерябиным Е.И. и Осиповым В.Ю., и Ю.Г. Кононенко и Г.П. Рузиным в 1991 году были предложены модификации этого метода. Сегодня существует много методик, когда проволочный шов сочетается со спицами, скобами, окружающими проволочными лигатурами и т.д.
Международные стандарты
Настоящая революция в челюстно-лицевой хирургии произошла в 1958 году, когда M. Muller, M. Allgower, R. Schneider, H. Willenegger организовали международную ассоциацию по изучению внутренней фиксации (AO/ASIF – Ardeitsgemeinschaft fur Osteosynthesefragen/Association for the Study of Internal Fixation – рабочее объединение по изучению вопросов остеосинтеза/ассоциация по изучению внутренней фиксации).
Согласно постулатам AO/ASIF, методика остеосинтеза подразумевает что:
1. используемые конструкции должны быть изготовлены из биоинертных сплавов металлов;
2. отломки костей должны быть анатомически точно сопоставлены и фиксированы;
3. использование щадящей хирургической техники обеспечивает сохранение кровоснабжения костных фрагментов и окружающих мягких тканей;
4. стабильная фиксация отломков обеспечивается межфрагментарной компрессией;
5. показано раннее применение функциональной нагрузки;
6. восстановление сократительной активности мышц и движения в суставе.
Сотрудники AO/ASIF также разработали и внедрили системы металлических пластин для остеосинтеза нижней челюсти:
· динамические компрессирующие пластины (Dynamic compression plates);
· реконструктивные (блокирующие) пластины (Locking reconstruction plates);
· блокирующие (стопорные) пластины (Locking plates 2.0 mm);
· универсальные пластины (Universal fracture plates);
· нижнечелюстные пластины (Mandible (Mandible plates 2.0 mm).
Ими были разработаны динамические компрессирующие пластины (DCP), посредством которых можно было создать компрессию между отломками для их первичного сращения. Конструкция этих пластин включает овальные отверстия со скошенными стенками, что позволяет сближать отломки при затягивании винтов. Применение динамических компрессирующих пластин позволило добиться стабильной внутренней иммобилизации, снизило число случаев замедленного сращивания отломков, и избавило от необходимости дополнительной фиксации. Но их применение все же не отменяет риск появления микротрещин в области линии перелома и развитие очагов остеопороза кости в месте контакта с пластиной.
Система блокирующих (стопорных) пластин и винтов (the locking plate/screw system) с резьбовой нарезкой в области отверстия пластин и головки фиксирующих винтов была разработана, чтобы предупредить появление некроза костной ткани под пластиной. Система обеспечивает жесткую фиксацию отломков кости с помощью пластины и пластины и винтов между собой – это помогает не допустить раскручивание винтов и избежать возможного смещения отломков во время закручивания винтов в отверстии пластины. Сама пластина располагается на некотором расстоянии от поверхности кости, что профилактирует развитие лизиса.
Зарубежные исследования не выявили существенных различий в эффективности и возможном развитии послеоперационных осложнений при остеосинтезе блокирующими пластинами с винтами и неблокирующими пластинами.
Еще одна система, разработанная экспертами АО/ASIF – это LCP (система блокируемых компрессирующих пластин с угловой стабильностью) представляет собой конструкцию из многоячеистых пластин с многочисленными отверстиями и состоит из двух частей: резьбовой для фиксации головки блокируемого винта и отверстия для создания динамической компрессии путем эксцентричного введения стандартных кортикальных или губчатых винтов.
Установка пластины предполагает наличие специальных инструментов и проводится по четко установленной технологии.
Если подгонка LCP по форме и рельефу наружной поверхности кости нижней челюсти проведена в соответствии с установленными требованиями, то это создает идеальные условия сращения отломков при остеосинтезе множественного оскольчатого перелома нижней челюсти различной локализации, при нагноении костной раны, травматическом остеомиелите, при переломе с возникновением дефекта костной ткани, переломе беззубых челюстей. Ограниченный контакт LCP с костью позволяет предупредить развитие некроза кости под пластиной.
Остеосинтез верхней челюсти
Челюстно-лицевым хирургам в своей практике приходится довольно часто сталкиваться с таким видом травмы, как перелом верхней челюсти. Чаще всего ее получают участники ДТП или конфликтных ситуаций с применением физической силы, а также любители экстремальных видов спорта. Перелом верхней челюсти – это невероятно опасный вид травмы, поскольку при нем повреждается непосредственно скелет лица пострадавшего, а это грозит не только появлением заметных эстетических дефектов, но и очень высоким риском развития целого ряда серьезнейших осложнений. К примеру, смещение отломков кости и/или сильный отек, который неизбежно образовывается при переломе, может привести к закрытию верхних дыхательных путей, в результате чего у человека развивается удушье. Кроме этого, костные отломки челюсти могут повредить крупные кровеносные сосуды, а также нервы головы и шеи. Поэтому очень важно понимать, что перелом верхней челюсти является крайне серьезной травмой, и отсутствие своевременного обращения за медицинской помощью может привести к необратимым последствиям, вплоть до летального исхода.
Перелом верхней челюсти сопровождается очень сильной болью, отеком в области повреждения тканей и нарушением симметрии лица; также, может быть заметно искривление верхнего зубного ряда. При любых признаках перелома челюстной кости следует немедленно обратиться за помощью к специалисту, ведь с каждым упущенным днем шансы восстановить первичную форму скелета лица становятся все ниже.
Перед началом лечения перелома доктор проводит необходимое обследование пациента, в рамках которого больной проходит рентгенографию или компьютерную томографию, после чего уже, в зависимости от нюансов имеющейся травмы, определяет наиболее подходящую методику проведения оперативного лечения перелома челюсти – остеосинтеза.
Оперативное лечение перелома верхней челюсти всегда проводится под анестезией, поэтому пациент не испытывает абсолютно никаких неприятных ощущений во время процедуры. Тщательно продезинфицировав оперируемую область пациента, доктор делает небольшой разрез мягких тканей ротовой полости и проводит прямые манипуляции на костных фрагментах – при помощи специальных металлических спиц или титановых пластин хирург соединяет отломки кости, надежно фиксируя их в правильном положении. В некоторых случаях перелома остеосинтез верхней челюсти может проводиться и без рассечения мягких тканей – такой метод применяется при несмещенных переломах. Выбор конкретной методики остеосинтеза верхней челюсти определяет челюстно-лицевой хирург в индивидуальном порядке, исходя из сложности повреждения костной ткани и наличия каких-либо осложнений. Однако в любом случае, доктор выбирает такой способ оперативного лечения перелома челюсти, при котором бы ему удалось восстановить анатомически правильную структуру челюстной кости и сохранить эстетический вид лица пациента.
После проведения остеосинтеза верхней челюсти зафиксированная в правильном положении кость быстро срастается. Если пациенту были установлены фиксирующие конструкции на челюстной кости, то после полного восстановления твердых и мягких тканей лицо пациента выглядит совершенно так же, как и до перелома.
В клинике Медистар остеосинтез верхней челюсти проводится по новейшим методикам с использованием ультрасовременных материалов. При лечении переломов лицевых костей наши доктора стремятся не только корректно восстановить поврежденные ткани, но и максимально сохранить красоту лица пострадавшего. А благодаря учету индивидуальных особенностей организма каждого пациента при составлении курса лечения нашим врачам удается сократить период послеоперационного восстановления и предотвратить развитие любых нежелательных последствий в будущем.
3228 зн
Рекомендации
Лечение переломов нижней челюсти предусматривает длительную иммобилизацию челюстей, что становится весомой психологической проблемой для пациента. Успех лечения напрямую зависит от того, насколько сплочённо действуют и серьезно относятся к процессу и врач, и пациент.
На весь срок сращения перелома пациенту назначается диета (челюстной стол №1 и №2), пищу разрешается принимать только в сметанообразной консистенции (хорошо разваренной и пропущенной через блендер). В большинстве случаев открывание рта невозможно, т.к. у пациента установлена межчелюстная резиновая тяга. Пища подается через зонды, трубки и поильники.
С момента двухчелюстного шинирования или остеосинтеза шины оставляют в среднем на 21 – 30 дней. Если у врача возникает уверенность в благоприятном течении процесса восстановления, то возможно уменьшение сроков ношения межчелюстной резиновой тяги.
Даже после снятия шин пациент не может полноценно открывать рот в течение 1-2 недель. Для восстановления функции жевательных и мимических мышц ему назначается миогимнастика.
Сравнительная оценка эффективности трех методов щадящей иммобилизации нижней челюсти при переломах
Г. А. Хацкевич д. м. н., профессор, завкафедрой стоматологии детского возраста с курсом челюстно-лицевой хирургии СПбГМУ им. акад. И. П. Павлова (Санкт-Петербург)
В. Г. Аветикян к. м. н., доцент кафедры стоматологии детского возраста с курсом челюстно-лицевой хирургии СПбГМУ им. акад. И. П. Павлова (Санкт-Петербург)
И. Г. Трофимов к. м. н., доцент кафедры стоматологии детского возраста с курсом челюстно-лицевой хирургии СПбГМУ им. акад. И. П. Павлова (Санкт-Петербург)
Чжан Фань врач, аспирант кафедры стоматологии детского возраста с курсом челюстно-лицевой хирургии СПбГМУ им. акад. И. П. Павлова (Санкт-Петербург)
И. Юань к. м. н., преподаватель Университета Шанхая (Шанхай, Китай)
В. Б. Некрасова д. м. н., профессор СПб МАПО (Санкт-Петербург)
Больные с травмами челюстно-лицевой области составляют около 30 % всех пациентов, находящихся на лечении в стационарах челюстно-лицевой хирургии, при этом переломы нижней челюсти составляют около 70—85 % от всех переломов костей лица (Ивасенко П. И., Журко Е. П., Чекин А. В., Конвай В. Д. и соавт., 2007; Инкарбеков Ж. Б., 2009; Bakardjiev A., Pechalova P., 2007).
Анализ опубликованных в научной литературе данных показал, что частота осложнений переломов нижней челюсти достигает от 10 до 41 % (Мубаркова Л. Н., 2008; Мирсаева Ф. З., Изосимов А. А., 2009), что не позволяет говорить об эффективности существующих методов лечения.
Важным патогенетическим звеном в развитии воспалительных осложнений при переломах нижней челюсти является нарушение местной иммунной защиты, регионального кровообращения и иннервации в зоне перелома, ухудшение гигиены полости рта и нарушение жевательной функции (Тимофеев А. А., 2004; Берхман М. В., Борисова И. В., 2007; Магомедгажиев Б. Г., 2008; Инкарбеков Ж. Б., 2009). Причем эти изменения может спровоцировать не только сама травма, но и неадекватные методы фиксации. Это особенно относится к круглым алюминиевым или к ленточным назубным шинам. Их наложение чрезвычайно травматично для пациента и опасно для хирурга в связи с возможностью ранения рук и инфицирования.
Кроме того, назубные шины, используемые в среднем в течение 30 суток, затрудняют гигиену ротовой полости и травмируют зубодесневую кайму. Это приводит к развитию резко выраженных воспалительных изменений в пародонте. Достаточно часто встречаются переломы нижней челюсти, при которых отсутствует смещение отломков, а подвижность невелика. В этом случае иммобилизация, которую обеспечивают назубные шины, оказывается избыточной. В связи с этим особую актуальность приобретает разработка щадящих методов иммобилизации.
Материал и методы исследований
Работа основывается на опыте лечения 90 пациентов с переломами нижней челюсти. Из них у 48 пациентов в качестве основного и вспомогательного (при операции остеосинтеза) метода фиксации использовался метод щадящей иммобилизации — межчелюстная фиксация с помощью несъемной ортодонтической техники (рис. 1).
Рис. 1а. Этап приклеивания назубных кнопок-брекетов Protekt. Иммобилизация нижней челюсти с помощью эластичных колец (наименее травматичный метод).
Рис. 1б. Этап приклеивания назубных кнопок-брекетов Protekt. Иммобилизация нижней челюсти с помощью эластичных колец (наименее травматичный метод).
В качестве методов сравнения использовались: иммобилизация отломков обвивными трансмаксиллярными швами — 18 пациентов (рис. 2).
Рис. 2а. Иммобилизация нижней челюсти с помощью двух проволочных обвивных швов.
Рис. 2б. Иммобилизация нижней челюсти с помощью двух проволочных обвивных швов.
Интермаксиллярное подвешивание с использованием ортодонтических мини-имплантатов — 24 пациента (рис. 3).
Рис. 3. Иммобилизация нижней челюсти с помощью внутрикостных имплантатов фиксаторов и эластичных колец.
Контрольная группа включала 16 лиц мужского пола (22,9 ± 1,2 года), практически здоровых.
В основной группе пациентов, где использовали брекеты Protekt и лингвальные кнопки, в качестве средств профилактики инфекционно-воспалительных осложнений связанных с травмой и с иммобилизацией нижней челюсти использовали биологически активные добавки (БАД) «Лесмин» для приема внутрь и индивидуальную гигиену полости рта с использованием зубной пасты «Фитолон».
Для диагностики и оценки результатов использовали клинико-рентгенологические иммунологические, индексно-гигиенические методы, электромиографию и допплеровскую флоуметрию для оценки сосудистой микроциркуляции.
Показания к выбору метода иммобилизации с помощью несъемной ортодонтической техники (Protect) следующие. Самостоятельный метод иммобилизация нижней челюсти, как альтернатива шинированию, применяли в следующих случаях: односторонние переломы без смещения или с незначительным смещением; двусторонние переломы без смещения или с незначительным смещением; перелом мыщелкового отростка без клинически определяемого и функционально значимого смещения (незначительное ограничение движений в височно-челюстном суставе вследствие болевых ощущений, прикус не нарушен). При двусторонних переломах нижней челюсти в ряде случаев, когда осуществляли остеосинтез титановыми пластинами, использовали брекет-фиксацию в качестве дополнительного метода (рис. 4).
Рис. 4. Двусторонний перелом нижней челюсти. Осуществлена иммобилизация с помощью остеосинтеза и брекет-фиксаторов.
В анализ были включены только те случаи, когда метод щадящей иммобилизации использовался в качестве основного метода фиксации отломков и пациентами в полной мере выполнялись предложенные авторами рекомендации по гигиене полости рта. Всего проанализировано 66 клинических случаев. Варианты переломов в процентах и их соотношение представлены на рисунке 5.
Рис. 5. Варианты переломов нижней челюсти при щадящих методах иммобилизации.
Результаты исследований
Больные всех 3 групп наблюдались в сроки от начала лечения и в течение 3 месяцев. Окончательная оценка результатов лечения проводилась через 3 месяца после травмы. Воспалительные осложнения учитывались на протяжении всего лечения.Консолидация отломков произошла у всех пациентов вне зависимости от метода щадящей иммобилизации. Нарушение прикуса выявили лишь у одного пациента, иммобилизация челюсти у которого осуществлялась с использованием ортодонтических мини-имплантатов. В данном случае восстановить прикус удавалось путем избирательной пришлифовки зубов. Эффективность лечения рассматриваемыми методами оказалась одинаковой.
Воспалительные осложнения отмечались при всех методах щадящей иммобилизации, при этом в случае использования несъемной ортодонтической техники (1-я группа) только у одного пациента (4,2 %) выявлен ограниченный остеомиелитический процесс за счет оставленного в щели перелома зуба с некрозом пульпы против 12,6 % при фиксации с помощью мини-имплантатов и 16,6 % при фиксации обвивными трансмаксиллярными швами (рис. 6).
Рис. 6. Частота (%) воспалительных осложнений при разных методах щадящей иммобилизации.
Во второй группе (использование мини-имплантатов) у 1 пациента произошло нагноение гематомы, а у 2 выявлен ограниченный остеомиелитический процесс. В третьей группе (обвивные трансмаксиллярные швы) у 2 пациентов отмечалось нагноение послеоперационных гематом в тканях дна полости рта и у одного пациента хронический травматический остеомиелит. Таким образом, в группе пациентов, у которых щадящая иммобилизация проводилась с использованием несъемной ортодонтической техники, количество воспалительных осложнений минимально, что обусловлено не только меньшей дополнительной травматизацией при процедуре иммобилизации отломков, но и системным применением БАД.
Анкеты для изучения самооценки качества жизни заполнялись пациентами через 1 месяц после травмы при снятии фиксирующих конструкций. Сравнительный анализ результатов исследования проводился в выборках по 12 пациентов от каждой группы. Изучение профилей «качества жизни» у пациентов при разных методах щадящей иммобилизации показало, что в меньшей степени качество жизни снижается у пациентов с переломами нижней челюсти при фиксации с использованием несъемной ортодонтической техники и мини-имплантатов (рис. 7).
Рис. 7а. Сравнительная оценка относительно здоровых респондентов профилей КЖ при разных способах щадящей иммобилизации. ОТМШ — обвивные трансмаксиллярные швы.
Рис. 7б. Сравнительная оценка относительно здоровых респондентов профилей КЖ при разных способах щадящей иммобилизации. ОМИ — ортодонтические мини-имплантаты.
Рис. 7в. Сравнительная оценка относительно здоровых респондентов профилей КЖ при разных способах щадящей иммобилизации. НОТ — несъемная ортодонтическая техника.
Через месяц после травмы самооценка качества жизни у пациентов с переломами нижней челюсти при щадящем методе иммобилизации с использованием несъемной ортодонтической техники по всем шкалам физического компонента здоровья и одной шкале психического компонента (жизнеспособность) выше, чем у пациентов при фиксации с использованием обвивных трансмаксиллярных швов.
При определении уровня гигиены полости рта регистрировали индекс гигиены Федорова — Володкиной (ИГФВ) и выраженность воспаления пародонта по состоянию папиллярно-маргигально-альвеолярного индекса (РМА), на первичном осмотре статистически значимых отличий у пациентов трех групп не установлено.
Наибольшие значения РМА установлены в группе пациентов, где фиксация отломков проводилась с применением обвивных трансмаксиллярных швов — 43,3 ± 2,4 %
В дальнейшем при исследовании через 7 дней уровень гигиены полости рта ухудшился вне зависимости от метода щадящей иммобилизации и был оценен во всех группах как неудовлетворительный. При исследовании через месяц во всех группах отмечен дальнейший рост ИГФВ, однако в группе с использованием несъемной ортодонтической техники повышение ИГФВ установлено в меньшей степени — 2,4 ± 0,03 против 2,64 ± 0,07 балла (р < 0,01) в группе, где фиксация проводилась с использованием ортодонтических мини-имплантатов.
Относительно исходных значений увеличение воспаления в динамике лечения отмечалось во всех группах пациентов. При этом наибольшие значения РМА установлены при заключительном исследовании в группе пациентов, где фиксация отломков проводилась с применением обвивных трансмаксиллярных швов — 43,3 ± 2,4 %, а наименьшие при предложенном нами щадящем методе иммобилизации с использованием несъемной ортодонтической техники — 26,4 ± 0,8 % (табл. № 1).
Таблица № 1. Сравнительный анализ динамики стоматологических индексов при щадящих методах иммобилизации нижней челюсти, используемых в качестве основных.
| № | группы | n | ИГФВ (баллы) | РМА (%) | ||||
| 1 раз | 2 раз | 3 раз | 1 раз | 2 раз | 3 раз | |||
| 1 | НОТ | 24 | 2,08±0,04 | 2,3 ±0,06 ** | 2,4±0,03 *** | 22,0±0,8 | 27,5 ±1,0 *** | 26,4±0,8 ** |
| 2 | ОМИ | 24 | 1,98±0,07 | 2,32±0,07 ** | 2,64±0,07 *** | 22,2±1,0 | 26,9±1,36 ** | 34,9±1,3 *** |
| 3 | ОТМШ | 18 | 2,17±0,04 | 2,35 ± 0,09 | 2,5±0,09 ** | 25,1±2,1 | 32,2±1,75 * | 43,3 ±2,4 *** |
| Р1-2 | >0,05 | >0,05 | <0,01 | >0,05 | ||||
| Р1-3 | >0,05 | >0,05 | >0,05 | >0,05 | ||||
Примечание: различия относительно первичного обследования статистически достоверны: * — р<0,05; ** — р<0,01; *** — р<0,001; 1-й раз при первичном осмотре; 2-й раз через 7 суток (при выписке); 3-й раз через 1 мес. (при снятии конструкций).
Такой результат связан с применением в группах сравнения хирургического вмешательства, стимулирующего воспалительную реакцию. На менее выраженное воспаление при заключительном исследовании могло оказать влияние и применение пациентами экспериментальной группы БАД «Лесмин» и использование зубной пасты «Фитолон».
Изучение факторов неспецифической защиты и местного иммунитета в ротовой жидкости пострадавших с переломами нижней челюсти при первичном обследовании выявило, что во всех группах отмечается достоверное по сравнению со здоровыми лицами снижение активности лизоцима на фоне активации мукозального иммунитета (повышение уровня иммуноглобулинов) при выраженном дисбалансе про- и противовоспалительных цитокинов (повышение ИЛ-8 и снижение ИЛ-4). При обследовании через неделю снижение активности лизоцима относительно исходных данных установлено только у пациентов с обвивными трансмаксиллярными швами (65,5 ± 2,1 против 73,1 ± 2,3 % при р < 0,01). В этой же группе установлены наиболее низкие показатели активности лизоцима и через месяц (63,6 ± 2,2 %), хотя при поступлении именно в этой группе активность лизоцима была наиболее высокой (рис. 8).
Рис. 8а. Динамика активности лизоцима и sIgА в группах пациентов. Примечание: НОТ — 1-я группа, ОМИ — 2-я группа, ОТМШ — 3-я группа.
Рис. 8б. Динамика активности лизоцима и sIgА в группах пациентов. Примечание: НОТ — 1-я группа, ОМИ — 2-я группа, ОТМШ — 3-я группа.
При исследовании через 7 дней в 1 и 2 группе уровень sIgА незначительно снизился, а в 3-й группе столь же незначительно повысился. Заключительное обследование через месяц показало незначительное снижение (нормализацию) sIgА в 1-й группе, где использовался предложенный нами метод щадящей иммобилизации с помощью несъемной ортодонтической техники — 56,1 ± 3,8 против 72,5 ± 5,78 мкг/мг белка (р < 0,01) и 77,7 ± 11,4 мкг/мг белка.
Исследования показали, что при использовании несъемной ортодонтической техники в качестве основного метода фиксации воспалительные, осложнения в зоне перелома выявляются в 4,2 % случаев
При исследовании через 7 дней IgG во всех группах все еще оставался на высоком уровне. На этом фоне только в экспериментальной группе пациентов было отмечено снижение IgМ до уровня контроля (с 2,3 ± 0,2 до 1,37 ± 0,1 мкг/мг белка, при р < 0,001). Исследование через месяц подтвердило нормализацию уровня IgМ только в экспериментальной группе, где использовался предложенный нами метод щадящей иммобилизации с использованием несъемной ортодонтической техники (1,38 ± 0,1 против 1,9 ± 0,13 и 2,49 ± 0,26 мкг/мг белка в группах сравнения). При этом через месяц в экспериментальной группе наиболее значительно снизился и IgG (3,77 ± 0,3 против 4,6 ± 0,45 и 5,0 ± 0,4 мкг/мг белка в группах сравнения).
При первичном обследовании уровень ИЛ-8 превосходил показатели контрольной группы в 9 раз, у отдельных пациентов он был более 5000 пг/мл, а ИЛ-4 в ряде случаев вообще не обнаруживался. На фоне столь масштабных изменений в регуляторах иммунного ответа наименьшие установлены у пациентов экспериментальной группы. Так, уже через 7 дней у них отмечается снижение ИЛ-8 (с 2707,9 ± 198,7 до 1916,3 ± 199,0 пг/мл, при р < 0,01), а при исследовании через месяц именно в этой группе отмечается наиболее низкий уровень ИЛ-8 (1488,2 ±183,3 против 1953,3 ± 202,1 и 2247,1 ± 304 пг/мл в группах сравнения) (рис. 9).
Рис. 9. Динамика ИЛ-8. Примечание: НОТ — 1-я группа, ОМИ — 2-я группа, ОТМШ — 3-я группа.
Динамика ИЛ-4 менее выраженна. В экспериментальной группе его количество в процессе лечения практически не меняется, оставаясь в 2 раза ниже, чем в контрольной группе, а в группах сравнения происходит его дальнейшее снижение. Через месяц у пациентов 1-й группы уровень ИЛ-4 составляет 2,7 ± 0,2 против 1,12 ± 0,4 и 1,0 ± 0,5 пг/мл в группах сравнения.
Таким образом, изучение активности лизоцима, мукозального иммунитета и уровня цитокинов в ротовой жидкости показало, что в ответ на перелом нижней челюсти организм отвечает реакцией острофазового воспаления, сопровождающейся снижением активности лизоцима на фоне активации мукозального иммунитета и выраженного дисбаланса про- и противовоспалительных цитокинов. При использовании разработанного нами метода щадящей иммобилизации на фоне системного приема БАД «Лесмин» нормализация нарушений протекает быстрее (в ряде случаев улучшение наступает уже через 7 дней), а при обследовании через месяц она более выраженна, что обусловлено менее травматичной методикой фиксации и системным приемом биомодулятора БАД «Лесмин».
Выводы
- В качестве опоры для мандибуло-максиллярной фиксации предлагается использовать несъемную ортодонтическую технику: назубные брекеты и лингвальные кнопки, что исключит хирургическое вмешательство, осложняющее течение восстановительного процесса в тканях пародонта, упростит и повысит эффективность лечения пациентов с переломами нижней челюсти.
- При использовании несъемной ортодонтической техники в качестве основного метода фиксации воспалительные осложнения в зоне перелома выявлены в 4,2 % случаев. При использовании зубной пасты «Фитолон» и БАД «Лесмин» зарегистрированы лучшие показатели в сравнении с контролем. ИГФВ 2,4 + 0,03 против 2,65+0,1 балла при Р<0,05, и снижение интенсивности воспаления пародонта РМА 26,4+ 0,1 против 36,8 + 2,0 % при Р < 0,001.
- Полученные нами данные подтверждают регулирующее действие цитокинов в развитии воспаления. Изначальное повышение ИЛ-8, как следствие травмы, физиологически обусловлено и стимулирует систему мукозального иммунитета, не оказывая отрицательного влияния на такой фактор неспецифической защиты полости рта, как лизоцим. Однако высокие значения ИЛ-8 через месяц отрицательно сказываются на восстановлении активности лизоцима. При этом снижение уровня противовоспалительного цитокина ИЛ-4, установленное на всех этапах исследования, сопровождается повышением активности лизоцима.
- Восстановление активности лизоцима на фоне снижения повышенных иммуноглобулинов ротовой жидкости и уменьшения степени дисбаланса между про- и противовоспалительными цитокинами приводит к уменьшению воспалительной реакции в пародонте и улучшению гигиенического состояния полости рта, что подтверждает эффективность использования зубной пасты «Фитолон» и системного применения БАД «Лесмин» у пациентов с переломами нижней челюсти на фоне щадящего метода иммобилизации с использованием несъемной ортодонтической техники.
- Сравнительный анализ в трех группах пациентов при щадящей иммобилизации показал, что в случае использования несъемной ортодонтической техники количество воспалительных осложнений минимально, что, видимо, обусловлено не только меньшей дополнительной травматизацией при процедуре иммобилизации отломков, но и системным применением БАД. При этом через месяц после начала лечения у этих пациентов самооценка качества жизни выше, чем при других методах щадящей иммобилизации.
- При разработанном нами методе щадящей иммобилизации нормализация выявленных нарушений местной неспецифической и иммунной защиты протекает быстрее — в ряде случаев улучшение показателей наступает уже через 7 дней (снижение sIgА, IgМ и ИЛ-8), а при обследовании через месяц нормализация более выраженна (снижение sIgА, IgМ и ИЛ-8 при повышении активности лизоцима), что обусловлено как менее травматичной методикой фиксации, так и системным приемом биомодулятора БАД «Лесмин», повышающего неспецифическую резистентность полости рта и обладающего антиоксидантным действием.